题目内容
12. 18世纪中期,为了解释燃烧现象,有人提出了“燃素说”,其主要观点有:
18世纪中期,为了解释燃烧现象,有人提出了“燃素说”,其主要观点有:①燃素是一种构成火的元素,火焰是自由的燃素,燃素能透过一切物体.
②一般条件下燃素被禁锢在可燃物中,是物体的一个成分.
③燃烧是可燃物中物体同燃素分解的过程.
(1)将汞装入密封容器中,置于火炉上加热,容器内形成丁质量增加的红色物质.请以上述燃素说的主要观点来解释质量增加的原因火焰中的燃素在加热过程能透过容器与汞结合形成红色物质,导致质量增加了.
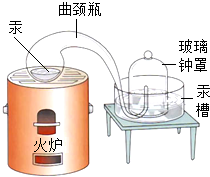
(2)法国化学家拉瓦锡也做了加热汞的实验(装置如图),他在实验前后称量了容器及其中物质的总质量.结果发现:反应前后总质量不变,且汞变成红色物质(后知是氧化汞)增加的质量等于容器中空气减少的质量.之后,拉瓦锡还将反应形成的氧化汞加强热,使之重新释放出气体,并将该气体与原来容器中剩余的气体混合,发现混合气体的性质与最初的空气相同.根据上述资料,回答:
①拉瓦锡实验是否支持燃素说,并说明理由不支持,因为从实验知汞增加的质量并非来自于燃素而是来自于空气.
②拉瓦锡实验中氧化汞受强热释放出的气体是氧气.
③拉瓦锡在实验中,均对反应前后的容器及其中物质的质量进行了称量,体现了他对质量守规律的重要认识.
分析 (1)根据信息:①燃素是一种构成火的元素,火焰是自由的燃素,燃素能透过一切物体.分析解题.
(2)①根据实验结果:反应前后总质量不变,且汞变成红色物质(后知是氧化汞)增加的质量等于容器中空气减少的质量.分析解题;
②根据汞燃烧生成氧化汞,可知增加的质量是氧气,所以氧化汞受强热释放出的气体是氧气;
③反应前后的容器及其中物质的质量进行了称量,体现了对质量守恒规律的认识.
解答 解:(1)通过信息①燃素是一种构成火的元素,火焰是自由的燃素,燃素能透过一切物体.可知将汞装入密封容器中,置于火炉上加热,容器内形成了质量增加的红色物质是:火焰中的燃素在加热过程能透过容器与汞结合形成红色物质,导致质量增加了.故答案为:火焰中的燃素在加热过程能透过容器与汞结合形成红色物质,导致质量增加了.
(2)①从实验知汞增加的质量并非来自于燃素而是来自于空气,而不是来自于燃素,所以拉瓦锡实验不支持燃素说.故答案为:不支持,因为从实验知汞增加的质量并非来自于燃素而是来自于空气.
②根据汞燃烧生成氧化汞,可知增加的质量是氧气,所以氧化汞受强热释放出的气体是氧气;故答案为:氧气.
③反应前后的容器及其中物质的质量进行了称量,体现了对质量守恒规律的认识.故答案为:质量守.
点评 本题是通过提取题目中所给信息解题,这就要求同学们细心阅读材料,并作出正确的理解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列实验操作正确的是( )
| A. | 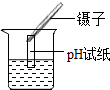 测定溶液的pH | B. | 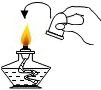 熄灭酒精灯 | C. | 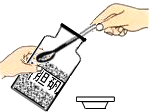 取用固体药品 | D. | 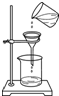 过滤操作 |
3.下列图象能正确反映对应变化的是实验室中用一氧化碳还原氧化铁( )
| A. | 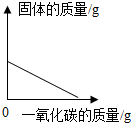 实验室用一氧化碳还原氧化铁 | |
| B. | 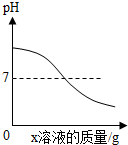 往氢氧化钙溶液中逐滴加入蒸馏水 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液 | |
| D. | 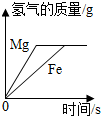 将足量粉末状金属分别与等质量、等质量分数的稀盐酸反应 |
17.溴化钙(CaBr2)可用作阻燃剂、制冷剂.溴化钙中溴的化合价为( )
| A. | +2 | B. | -2 | C. | +1 | D. | -1 |
1. 实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
(1)这瓶无色液体不可能是蒸馏水,理由是由标签知该液体是混合物,而蒸馏水为纯净物.
(2)为验证该液体是什么,进行了如表实验:
(3)如果该液体是过氧化氢溶液,则上表步骤一中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
 实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?(1)这瓶无色液体不可能是蒸馏水,理由是由标签知该液体是混合物,而蒸馏水为纯净物.
(2)为验证该液体是什么,进行了如表实验:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少量二氧化锰粉末. | 该液体不是 过氧化氢溶液. | |
| 步骤二:另取该液体适量于试管中,用胶头滴管(或滴管)向其中加入少量氯化钡溶液. | 产生白色沉淀 | 该液体是 稀硫酸. |
2.某小组同学外出野炊,所带的部分物品如表所示:
(1)从合理膳食,均衡饮食的角度分析,他们带的食物中还缺少水和水果或蔬菜.
(2)到了目的地,他们发现装食盐和苏打的瓶子忘记了做标记,可用所带物品食醋来鉴别.
(3)做饭过程中,小红把炉灶里的树枝架空,使其燃烧更旺,原理是增大树枝与氧气的接触面积.
(4)味精是烹调中常用的鲜味调味品,它的主要成分是谷氨酸钠.管氨酸钠低温时不易溶解,在温度T≥100℃时,长时间加热会转变成人体有害物质,根据以上信息,请写出一条食用味精时的注意事项在食物出锅前加入.
(5)野炊结束后应及时把火熄灭,写出一种可采用的灭火方法用水浇灭或用泥土将燃烧物覆盖起来.
| 食物 | 馕、羊肉、鲫鱼、豆腐 |
| 调料 | 食盐、苏打、砂糖、食醋、味精、酱油、食用油 |
(2)到了目的地,他们发现装食盐和苏打的瓶子忘记了做标记,可用所带物品食醋来鉴别.
(3)做饭过程中,小红把炉灶里的树枝架空,使其燃烧更旺,原理是增大树枝与氧气的接触面积.
(4)味精是烹调中常用的鲜味调味品,它的主要成分是谷氨酸钠.管氨酸钠低温时不易溶解,在温度T≥100℃时,长时间加热会转变成人体有害物质,根据以上信息,请写出一条食用味精时的注意事项在食物出锅前加入.
(5)野炊结束后应及时把火熄灭,写出一种可采用的灭火方法用水浇灭或用泥土将燃烧物覆盖起来.
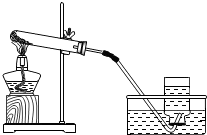 如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.
如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.