题目内容
6.某化学兴趣小组同学进行以下两个实验:实验一:配制溶质质量分数为10%的NaCl溶液100g
实验二:称取10.0g粗盐进行提纯,粗盐除NaCl外,还含有Mg2+、SO42-、Ca2+以及泥沙等杂质,为了有效将粗盐中杂质除尽,该小组同学设计了实验操作如下:(X为水)
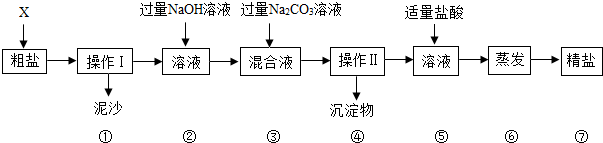
(1)实验一的操作步骤为:计算、称量、溶解、装瓶存放(按顺序填写).
(2)实验二中操作步骤Ⅰ所需玻璃仪器有漏斗、玻璃棒和烧杯;
在②中加入过量NaOH溶液的目的是除净粗盐中的镁离子;
在⑤中加入适量盐酸的目的是除去过量的氢氧化钠和碳酸钠;
按以上操作所得精盐中仍含有一种杂质离子是SO42-,若除去该杂质离子,可在上述步骤B(填下列选项),加入过量的BaCl2溶液.
A、①②B、②③C、③④D、④⑤E、⑤⑥F、⑥⑦
分析 (1)配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解,据此进行分析判断;
(2)步骤Ⅰ是分离固体与液体,是过滤操作;根据氢氧化钠能与镁离子结合成沉淀来分析;根据盐酸的化学性质来分析;根据添加的试剂以及除杂质的方法来分析.
解答 解:(1)配制100g溶质质量分数为10%的NaCl溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.故填:计算、称量、溶解、装瓶存放;
(2)过滤操作需要用到的玻璃仪器是漏斗、玻璃棒和烧杯;故填:漏斗、玻璃棒和烧杯;
氢氧化钠与镁离子结合成了氢氧化镁白色沉淀,故填:除净粗盐中的镁离子;
适量的盐酸可以除去剩余的氢氧化钠和过量的碳酸钠,故填:除去过量的氢氧化钠和碳酸钠;
以上试剂没有除去硫酸根离子,所以要加入过量的氯化钡溶液,并利用碳酸钠将过量的钡离子除去,故填:SO42-;B.
点评 粗盐提纯是经常考查的内容,其中要涉及到化学方程式的书写、过滤操作、杂质的除去等内容,需要同学们对此内容了然于心.

练习册系列答案
相关题目
16.能将碳酸钠溶液、氢氧化钠溶液、硝酸银溶液一次性鉴别出来的试剂是( )
| A. | 紫色石蕊溶液 | B. | 无色酚酞溶液 | C. | 稀盐酸 | D. | 氢氧化钙溶液 |
14.有a、b、c三种金属,如果把a、b、c分别放入足量硫酸溶液中,a完全溶解,并产生气泡,b、c不反应,如果将b、c分别放入硫酸铜溶液中,过一会儿,在c的表面有红色物质出现,b没有变化,则a、b、c的金属活动性正确的是( )
| A. | a>b>c | B. | c>a>b | C. | a>c>b | D. | b>c>a |
1.6.5g不纯的锌样品(只含一种杂质),与足量盐酸反应后,共得到0.18g氢气,此样品中含有的一种杂质可能是( )
| A. | Cu | B. | Mg | C. | Al | D. | Fe |
11.小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的PH变化关系如图2所示,下列说法正确的是( )
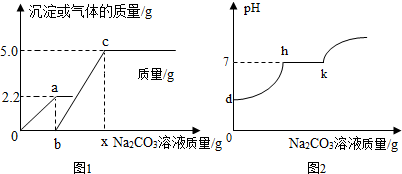

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为53 | |
| C. | 图1中c时,溶液中的溶质有两种 | |
| D. | 图1中o→a段反应过程中溶液的PH变化情况可用图2中h→k段表示 |