题目内容
15.现有a、b、c三种金属,将a、b分别放入稀硫酸及c的硝酸盐溶液中,现象如下所示| a | b | |
| 在稀硫酸中 | 无反应 | 溶解并放出气体 |
| 在C的硝酸盐溶液中 | 表面上析出c | 表面上析出c |
| A. | a,b,c | B. | c,b,a | C. | b,a,c | D. | a,c,b |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答 解:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,a、b、c三种金属,将a、b分别放入稀硫酸,a无反应,说明了活动性氢>a;b溶解并放出气体,说明了活动性b>氢;
位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,将a、b分别放入C的硝酸盐溶液中,a无反应,说明了活动性c>a;b无反应,说明了活动性c>b;故a、b、c化学性质由强到弱的顺序是c b a.
故选:B.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
相关题目
5.下列氢氧化铜的性质中属于碱的化学性质的是( )
| A. | 蓝色固体 | B. | 难溶于水 | ||
| C. | 能与盐酸反应 | D. | 能使无色酚酞变红 |
20.重金属离子有毒性.实验室有甲、乙两种废液,均有一定毒性.甲废液经化验呈碱性,主要有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低.乙废液中可能含有的离子是( )
| A. | Cu2+和SO42- | B. | Cu2+和Cl- | C. | K+和SO42- | D. | Ag+和NO3- |
7.下列实验过程中与图象描述相符的一组是( )
| A. |  两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 | |
| B. |  向等质量的镁、锌中分别加入稀盐酸 | |
| C. |  向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 | |
| D. |  室温下,向一定质量的饱和石灰水中加入氧化钙 |
5. 某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液.实验中是“滴入植物油”的目的是隔绝氧气.
实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈碱性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
实验方法:
①取上述氢氧化钠溶液分为AB两等份
②B溶液中加足量的水稀释
③分别滴加等量酚酞
观察到的现象A溶液:溶液变成红色且过一会后红色消失
B溶液:溶液变成红色且过一会后红色不消失
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如表).
(4)表中X=7.
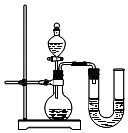
(5)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据U形管中左边液面下降判断氢氧化钠溶液与稀盐酸发生了中和反应.
 某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.方案一:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液.实验中是“滴入植物油”的目的是隔绝氧气.
实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈碱性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象.设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
实验方法:
①取上述氢氧化钠溶液分为AB两等份
②B溶液中加足量的水稀释
③分别滴加等量酚酞
观察到的现象A溶液:溶液变成红色且过一会后红色消失
B溶液:溶液变成红色且过一会后红色不消失
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
(5)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据U形管中左边液面下降判断氢氧化钠溶液与稀盐酸发生了中和反应.


 室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图:
室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图: