题目内容
19.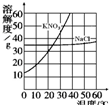 分析KNO3、NaCl两种物质的溶解度曲线,回答下列问题.
分析KNO3、NaCl两种物质的溶解度曲线,回答下列问题.(1)10℃时,KNO3物质的溶解度是20g;
(2)20℃时,在100g水中溶解25g KNO3物质,得到KNO3溶液的溶质质量分数为20%;
(3)不能用降温的方法使氯化钠结晶,是因为氯化钠的溶解度受温度的影响较小.
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;10℃时,KNO3物质的溶解度是20g;20℃时,硝酸钾的溶解度是30g,因此在100g水中溶解25gKNO3物质,得到KNO3溶液的溶质质量分数=$\frac{25g}{125g}×100%$=20%;不能用降温的方法使氯化钠结晶,是因为氯化钠的溶解度受温度的影响较小.
解答 解:(1)由溶解度曲线可知:10℃时,KNO3物质的溶解度是20g;故答案为:20;
(2)10℃时,KNO3物质的溶解度是20g;20℃时,硝酸钾的溶解度是30g,因此在100g水中溶解25gKNO3物质,得到KNO3溶液的溶质质量分数=$\frac{25g}{125g}×100%$=20%;故答案为:20%;
(3)不能用降温的方法使氯化钠结晶,是因为氯化钠的溶解度受温度的影响较小,故答案为:氯化钠的溶解度受温度的影响较小;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
7.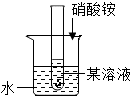 如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
 如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )| A. | 硝酸钾 | B. | 氯化钠 | C. | 氯化氢 | D. | 熟石灰 |
14.下列有关分子、原子和离子的说法正确的是( )
| A. | 分子是保持物质性质的一种粒子 | |
| B. | 物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变 | |
| C. | 分子、原子、离子都可以直接构成物质 | |
| D. | 具有相同质子数的微粒一定属于同种元素 |
4.生石灰是一种传统的建筑材料,俗称“石灰”.工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究.
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】Ⅰ.只有氧化钙Ⅱ.只有碳酸钙Ⅲ.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立.乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
【思考】使用“石灰”的建筑工地上常有一个大的石灰池,使用“石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用.长期使用的石灰池内壁会逐渐增厚,其主要原因是氢氧化钙吸收空气中的二氧化碳形成难溶的碳酸钙.
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】Ⅰ.只有氧化钙Ⅱ.只有碳酸钙Ⅲ.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立.乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,过滤 取滤液滴加无色酚酞溶液 ②取样品滴加稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅲ成立 |
11.下列试剂中,能一次性将KOH溶液、稀硫酸、CaCl2溶液鉴别出来的是( )
| A. | 稀盐酸 | B. | K2CO3溶液 | C. | 无色酚酞 | D. | NaNO3溶液 |
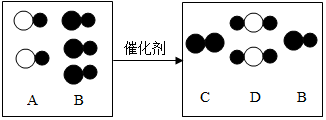
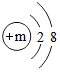 ,其微粒符号可表示为X2,则m的值为8.
,其微粒符号可表示为X2,则m的值为8.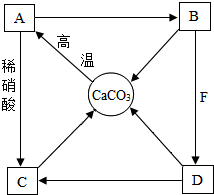 A~F是初中化学常见物质,A、B、C、D和CaCO3均含有同一种元素,其中B常用于改良酸性土壤,胃液中含有F.它们之间的转化关系如图所示,“→”表示相互转化.请回答:
A~F是初中化学常见物质,A、B、C、D和CaCO3均含有同一种元素,其中B常用于改良酸性土壤,胃液中含有F.它们之间的转化关系如图所示,“→”表示相互转化.请回答: