题目内容
15.准确理解化学概念的内涵对于学好化学非常重要,下列说法错误的是( )| A. | 空气污染指数是横量空气质量的重要指标,指数越小空气质量越好 | |
| B. | 催化剂可以改变化学反应的快慢,但反应前后自身的性质,质量一定都不变 | |
| C. | 氧化物一定都属于化合物 | |
| D. | 有氧气参与的化学反应,一定都属于氧化反应 |
分析 A、空气污染指数指空气被污染的程度,指数越大,空气污染越严重;
B、根据催化剂的定义和催化剂的特点进行分析解答;
C、有的氧化物不一定都属于化合物;
D、物质跟氧气发生的反应都是氧化反应.
解答 解:A、空气污染指数指空气被污染的程度,指数越大,空气污染越严重,指数越小空气质量越好,故A正确;
B、有的催化剂能加快反应速度,有的催化剂能减慢反应速度,一定能改变反应速率,催化剂在化学反应中本身的质量和化学性质在反应前后不变,故B正确;
C、氧化物不一定是化合物比如氧气是氧化物是单质,故C错误;
D、物质和氧气发生的化学反应都属于氧化反应;故D正确.
故选C.
点评 本题主要考查课本基本的概念和基础知识,难度不大,但容易混淆,细心解答.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
5.氧化汞受热时的变化可用下图表示,据图得出的下列结论中错误的是( )


| A. | 这一变化是化学变化 | |
| B. | 氧化汞是由氧化汞分子构成的 | |
| C. | 汞是由汞分子构成的 | |
| D. | 这一变化说明在化学变化中原子不能再分 |
3.下列物质能在pH=13的无色溶液中大量共存的是( )
| A. | HCl、AgNO3、Na2CO3 | B. | NaNO3、KNO3、NH4Cl | ||
| C. | K2SO4、K2CO3、NaOH | D. | KMnO4、CuSO4、NaNO3 |
20.用一氧化碳在加热的条件下还原氧化铜,发现已制得的铜又很快变黑了,你推测产生这种现象的原因是( )
| A. | 温度太低 | |
| B. | 反应开始时,没有把试管内的空气排干净 | |
| C. | 试管口倾斜了 | |
| D. | 铜没有在一氧化碳气流中冷却而又被空气中氧气所氧化 |
7.治污水是“五水共治”内容之一.根据国家标准,废水排放时铅元素的含量不允许超过1.0毫克/升.蓄电池生产企业往往采用化学沉淀法处理Pb2+,其中以氢氧化物沉淀法应用较多.根据下表信息,沉淀剂除了NaOH外,还可使用的两种钠盐是碳酸钠和硫化钠.
20℃时,各种铅的化合物在水中的溶解度
20℃时,各种铅的化合物在水中的溶解度
| 物质 | 溶解度/克 | 物质 | 溶解度/克 |
| Pb(NO3)2 | 54.3 | PbCO3 | 7.3×10-5 |
| Pb(OH)2 | 1.6×10-4 | PbS | 6.8×10-13 |
4.请你利用学到的化学知识来判断下列突发事件处理不当的是( )
| A. | 室内着火被困,立即用湿毛巾堵住口鼻,匍匐前进,寻找安全出口 | |
| B. | 发现有人煤气中毒,立即打开门窗,关闭阀门,将中毒人员转移到空气新鲜的地方 | |
| C. | 浓碱溅到皮肤上,立即涂抹稀硫酸 | |
| D. | 误服食品袋中的干燥剂(生石灰),立即喝食醋 |
5.市面上出售的“水壶一次净”能较好地除去水壶中的水垢,为确定它的成分和使用范围,某同学通过以下实验进行探究:(1)取少量样品加入锌粒后,有气泡产生,生成的气体可燃烧并产生淡蓝色火焰.(2)另取少量样品滴加硝酸银后,出现白色沉淀,再滴加稀硝酸沉淀不消失.经实验,该同学关于“水壶一次净”的下列结论与推断中合理的是( )
| A. | 主要成分是盐酸,实验(1)多余 | |
| B. | 主要成分是盐酸,实验(2)多余 | |
| C. | 主要成分是盐酸,对金属无腐蚀作用,可放心使用 | |
| D. | 主要成分是盐酸,对金属有腐蚀作用,应适量使用 |
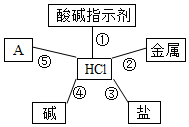 归纳是学习的重要方法.某同学学习了盐酸后总结如图所示的反应关系,试回答.
归纳是学习的重要方法.某同学学习了盐酸后总结如图所示的反应关系,试回答.