题目内容
20.氢能源具有诱人的前景,请联系有关知识回答下列问题(氢气的燃烧热值为1.5ⅹ108J/kg)(1)所谓氢能源是指氢气燃料,它与其他能源相比,具有三大显著优点:资源丰富、燃烧热值高、燃烧产物是水无污染.
(2)完全燃烧2kg氢气生成水18千克?同时放出热量是3×108焦?
(3)通常情况下,氢气的获得是从水电解水中得到的,需要消耗一定的常规能源,比如:“220V,50A”的条件下,需24小时才能得到1千克氢气,请写出电解水的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,并通过计算说明这种方法是否可取?
(4)为了获得氢能源,必须采用先进的方法,以下所提供的方法中,你认为可行的是C
A、由热电站提供电力电解水 B、改进以焦炭和水制水煤气的方法
C、利用太阳能分解水 D、使用灼热的铁 和水蒸气反应制得.
分析 (1)根据氢气燃烧的特点分析;
(2)根据热值物理量的含义分析,根据化学方程式,已知氢气质量求水的质量;
(3)根据题意设出未知量,写出方程式,然后再计算相关物质的相对分子质量和已知量、未知量,在列出比例式求解,最后简明的写出答案;
(4)据原题“目前科学家们认为高效率制氢的基本途径是利用太阳能.如果能用太阳能制氢,那就等于把无穷无尽的,分散的太阳能转变成了高度集中的干净能源了,意义十分重大”可判断.
解答 解:(1)氢气资源丰富,燃烧热值高,燃烧产物是水无污染,因此比其它能源有显著优点;
(2)1.5×108焦/千克,它的物理量意义为燃烧一千克氢气放出的热量为1.5×108焦.
设生成水的质量为x.
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 36
2kg x
$\frac{4}{36}$=$\frac{2kg}{x}$
x=18kg
放出的热量为1.5×108焦/千克×2kg=3×108焦.
(3)水电解的方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
已知工作电压和通过的电流,利用W=UIt求消耗的电能.消耗的电能:W电=UIt=220V×50A×24×60×60s=9.5×108焦,因为燃烧一千克氢气放出的热量为1.5×108焦.
所以这种方法不可取.
(4)据原题“目前科学家们认为高效率制氢的基本途径是利用太阳能.如果能用太阳能制氢,那就等于把无穷无尽的,分散的太阳能转变成了高度集中的干净能源了,意义十分重大”可判断该题中的C选项是正确的;
故答案为:(1)资源丰富、燃烧热值高、燃烧产物是水无污染;
(2)18kg;3×108焦;
(3)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;不可取;
(4)C.
点评 本题考查氢气燃烧的特点及根据化学方程式的简单计算,属基础知识考查.

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案| A. | CO 酸性氧化物 | B. | Mg(OH)Cl 碱 | ||
| C. | NaH 2PO4 酸式盐 | D. | CuSO4•5H2O 混合物 |
①O2②Mg2+③SO2④
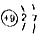 ⑤
⑤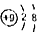
| A. | ①可表示两个氧原子 | B. | ③中硫元素的化合价为+4 | ||
| C. | ②和⑤均表示阳离子 | D. | ④和⑤表示的微粒化学性质相同 |
| A. | CO(CO2)通过灼热的氧化铜 | |
| B. | 氯化钙溶液(盐酸)加过量的碳酸钙后过滤 | |
| C. | NaOH溶液(Na2CO3)加适量稀盐酸 | |
| D. | 铁粉(氧化铜粉末)加入足量稀硫酸后过滤 |
| A. | FeCl3 | B. | BaCl2 | C. | CO2 | D. | KOH |
| 操作 | 现象 | 结论 |
| 分别打开瓶盖 | 其中一瓶瓶口上方产生白雾,另一瓶无明显变化 | 瓶口上方产生白雾的是浓盐酸,无明显变化的是浓硫酸 |
 石墨烯是“新材料之王”
石墨烯是“新材料之王”
