题目内容
14.下列实验现象描述正确的是( )| A. | 铜丝加热表面有红色变成黑色 | |
| B. | CO2通入CaCl2溶液中会生成白色沉淀 | |
| C. | 木炭在空气中燃烧产生刺激性气体 | |
| D. | 铁锈加稀盐酸中,得到浅绿色溶液 |
分析 A、根据铜和氧气加热产生黑色的氧化铜分析;
B、根据二氧化碳和氯化钙不能反应分析;
C、根据碳和氧气产生二氧化碳分析;
D、根据铁锈的成分是氧化铁,氧化铁和稀盐酸反应产生氯化铁是黄色的溶液分析.
解答 解:A、铜和氧气加热产生黑色的氧化铜,故描述正确;
B、二氧化碳和氯化钙不能反应,因此无明显现象,故描述错误;
C、碳和氧气产生二氧化碳,二氧化碳是无色无味的气体,故描述错误;
D、铁锈的成分是氧化铁,氧化铁和稀盐酸反应产生氯化铁是黄色的溶液,铁和盐酸反应产生氯化亚铁是浅绿色的溶液,故描述错误;
故选项为:A.
点评 本题难度不大,掌握常见物质在空气中或在氧气中燃烧的实验现象是解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.如图是模拟海水制盐的流程
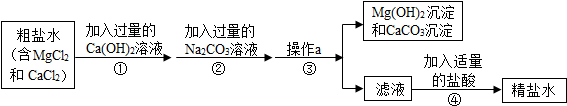
操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
【反思与拓展】为了使制得的精盐水只含有氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶操作.
组成探究】
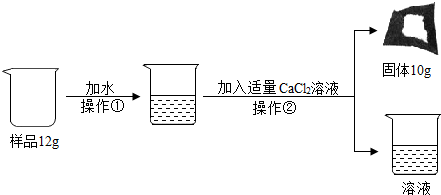
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)

操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 产生白色沉淀 | 猜想三是正确的 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液(填指示剂) | 溶液变红色 |
组成探究】
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
9.甲烷(CH4)燃烧的化学反应的微观示意图如下图所示,则下列说法正确的是( )
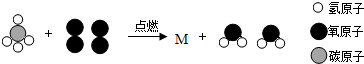

| A. | 反应前后分子种类、数目均不变 | B. | 该反应中各物质均为化合物 | ||
| C. | 该反应中,反应物的质量比是1:2 | D. | 该反应为氧化反应 |
19.下列有关物质的检验、鉴别、除杂、分离所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 检验一瓶气体是否为CO2 | 燃着的木条 |
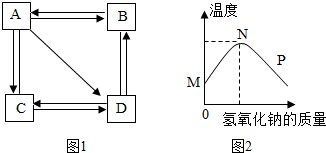
| B | 鉴别氢氧化钠溶液和饱和石灰水 | 升高温度 |
| C | 分离铁粉和铜粉混合物 | 稀硫酸 |
| D | 除去NaOH溶液中的Na2CO3 | 氢氧化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
3.区分下列各组物质的两种方法都正确的是( )
| 需区分物质 | 方法一 | 方法二 | |
| A | 食盐和纯碱 | 闻气味 | 测pH |
| B | 黄铜和黄金 | 观察颜色 | 用稀盐酸 |
| C | 碳酸氢铵和磷矿粉 | 加水溶解 | 加熟石灰研磨 |
| D | 氢氧化钙和氢氧化钠 | 加酚酞溶液 | 通入二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
4.下列有关生产、环保、资源问题叙述错误的是( )
| A. | 塑料的使用对人类来说有利也有弊 | |
| B. | 长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用 | |
| C. | 煤气的主要成分是氢气、甲烷和一氧化碳 | |
| D. | 煤和石油是不可再生资源,必须综合利用以提高利用率 |