题目内容
9.小红同学进行酸碱中和反应实验,反应后为确定稀盐酸和氢氧化钠溶液是否刚好完全反应,她将少量反应后的溶液,倒入一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是她得出“两种物质已恰好完全中和”的结论.(1)写出该中和反应的化学方程式NaOH+HCl═NaCl+H2O;
(2)小霞认为小红的结论不准确,她认为除了“恰好中和”外还有一种假设,这种假设是稀盐酸过量;
(3)请你设计实验,探究小霞的假设是否成立.
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入紫色石蕊试液 | 试液不变红 | 恰好中和 |
分析 盐酸和氢氧化钠反应生成氯化钠与水.在此反应类型中,若盐酸过量,溶液显酸性,滴加酚酞溶液时,酚酞也不显色.
解答 解:解答此题有三个关键:一是要明确中和反应过程中溶液酸碱性的变化情况,滴加的稀盐酸过少,溶液显碱性;恰好完全反应,溶液显中性;滴加的稀盐酸过多,溶液显酸性.二是要明确酚酞不变色,溶液可能显中性,也有可能显酸性.三是要明确第(3)问中的“另设计一个实验”应在已经知道溶液“要么恰好完全中和,要么盐酸过量”的基础上考虑实验方法.
故答案为:(1)NaOH+HCl═NaCl+H2O
(2)稀盐酸过量;
(3)以下方法任写一种均可:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入紫色石蕊试液 | 试液不变红 | 恰好中和 |
| 取反应后的溶液于试管中,加入紫色石蕊试液 | 试液变红 | 盐酸过量 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 无气泡产生 | 恰好中和 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 有气泡产生 | 盐酸过量 |
| 取反应后的溶液于试管中,加入锌粒等活泼金属 | 无气泡产生 | 恰好中和 |
| 取反应后的溶液于试管中,加入锌粒等泼泼金属 | 有气泡产生 | 盐酸过量 |
点评 中和反应的实质是氢离子和氢氧根离子结合成水的过程.中和反应不属于基本反应类型.它的基本类型为复分解反应.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
19.化学实验操作的正确性、规范性是实验成败的关键,下列实验操作中不正确的是( )
| A. |  倾倒液体药品 | B. | 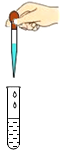 滴加稀盐酸 | C. |  给液体加热 | D. | 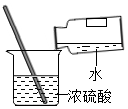 稀释浓硫酸 |
17.化学式“CO2”表示意义错误的是( )
| A. | 二氧化碳这种物质 | |
| B. | 一个二氧化碳分子 | |
| C. | 二氧化碳是由碳、氧两种元素组成 | |
| D. | 二氧化碳是由一个碳原子和两个氧原子组成 |
14.在FeSO4和CuSO4的混合溶液中加入过量的锌粉,充分反应得到一定量固体.对固体成分的说法正确的是( )
①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe.
①一定含有Zn ②一定含有Fe ③一定含有Cu ④可能含有Zn ⑤可能含有Fe.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ①②④ |
18.下列做法不恰当的是( )
| A. | 氮气用于保护灯丝 | B. | 氧气用于医疗急救 | ||
| C. | 肥皂水用于软化硬水 | D. | 石墨用作机器润滑剂 |
 今年为增强内需促进经济发展,家用汽车发展较快.
今年为增强内需促进经济发展,家用汽车发展较快.