题目内容
氧化铜和炭粉的混合物3.44克加热后完全反应,将生成的气体通入过量的澄清石灰水中,可得白色沉淀2.0克,试求:
(1)混合物中氧化铜多少克?
(2)混合物中炭的质量分数.
(1)混合物中氧化铜多少克?
(2)混合物中炭的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据题意,发生的反应是:2CuO+C
2Cu+CO2↑和 CO2+Ca(OH)2═CaCO3↓+H2O,二者之间可通过二氧化碳相联系,根据反应的方程式可以找出氧化铜、碳和碳酸钙之间的关系,利用关系式法计算较为简便.
| ||
解答:解:(1)根据题意,由发生的反应:2CuO+C
2Cu+3CO2↑和 CO2+Ca(OH)2═CaCO3↓+H2O可以得出氧化铜、碳和碳酸钙之间的关系是:2CuO~C~CaCO3.
设原混合物中氧化铜和炭粉的质量分别是x、y
则 2CuO~C~CaCO3
160 12 100
x y 2.0g
=
解得:x=3.2g
=
解得:y=0.24g
(2)混合物中炭的质量分数=
×100%=7.0%
答:(1)混合物中氧化铜为3.2g;
(2)混合物中炭的质量分数为7.0%.
| ||
设原混合物中氧化铜和炭粉的质量分别是x、y
则 2CuO~C~CaCO3
160 12 100
x y 2.0g
| 160 |
| x |
| 100 |
| 2.0g |
解得:x=3.2g
| 12 |
| y |
| 100 |
| 2.0g |
解得:y=0.24g
(2)混合物中炭的质量分数=
| 0.24g |
| 3.44g |
答:(1)混合物中氧化铜为3.2g;
(2)混合物中炭的质量分数为7.0%.
点评:本题在计算时,利用关系式法计算比较简便,解题的关键是利用反应的方程式所表示的意义找出反应关系式.

练习册系列答案
相关题目
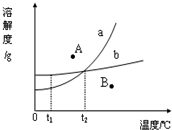 如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:
如图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:

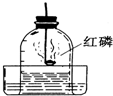 如图所示装置(燃烧匙中盛放的是红磷)可用于测定空气中氧气的含量,将红磷点燃后迅速塞好橡皮塞.回答一下问题.
如图所示装置(燃烧匙中盛放的是红磷)可用于测定空气中氧气的含量,将红磷点燃后迅速塞好橡皮塞.回答一下问题.