题目内容
5. 某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,他取出50g该溶液.逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,他取出50g该溶液.逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:(1)Cu(OH)2质量为4.9g;
(2)计算硫酸铜溶液溶质质量分数(请写出计算过程).
(3)在实验过程中,以下说法正确的是CD.
A、0至b段溶液中溶质质量逐渐增加
B、a、b、c点对应的溶液中溶质均为一种
C、向c点对应的溶液中滴加酚酞溶液,溶液变红
D、整个过程中,溶液中氢元素的质量一直在增加.
分析 硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)由图中数据可知,Cu(OH)2质量为4.9g.
故填:4.9.
(2)设硫酸铜质量为x,
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓,
160 98
x 4.9g
$\frac{160}{x}$=$\frac{98}{4.9g}$,
x=8g,
硫酸铜溶液溶质质量分数为:$\frac{8g}{50g}$×100%=16%,
答:硫酸铜溶液溶质质量分数为16%.
(3)在实验过程中,以下说法正确的是 CD.
A、由CuSO4+2NaOH=Na2SO4+Cu(OH)2↓,
160 142
可知,当有160份质量的硫酸铜反应时生成142份质量的硫酸钠,因此随着反应的进行,0至b段溶液中溶质质量逐渐减小,该选项说法不正确;
B、a点对应的溶液中溶质是硫酸铜和硫酸钠,b点对应的溶液中溶质是硫酸钠,c点对应的溶液中溶质是氢氧化钠和硫酸钠,该选项说法不正确;
C、c点时溶液中含有氢氧化钠,氢氧化钠溶液显碱性,能使酚酞试液变红色,因此向c点对应的溶液中滴加酚酞溶液,溶液变红,该选项说法正确;
D、硫酸铜和氢氧化钠反应时,氢氧化钠中的氢元素转化成氢氧化铜沉淀中的氢元素,而溶剂水中的氢元素进入溶液,b~c过程中,氢氧化钠溶液中的氢元素全部进入溶液,因此整个过程中,溶液中氢元素的质量一直在增加,该选项说法正确.
故填:CD.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

| A. | 冰雪融化 | B. | 粮食酿酒 | C. | 汽油挥发 | D. | 瓷碗破碎 |
| A. |  测溶液pH | B. |  取用固体药品 | C. |  稀释浓硫酸 | D. |  读出液体的体积 |
| A. | 食醋除水垢 | B. | 生石灰作干燥剂 | ||
| C. | 配制农药波尔多液 | D. | 汽油洗除衣物上少量油污 |
| 每100g含有的营养成分 | 糖类 | 脂肪 | 蛋白质 | 钙 |
| 7.6g | 7.8g | 7.4g | 201mg |
(2)当老年人缺钙时,可能导致骨质疏松.
(3)小麦在种植过程中出现茎叶细小症状,同时有倒伏现象时,应施用复合肥,下列属于复合肥的是C(填序号).
A.KCl B.NH4NO3 C.KNO3.
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 浓氯化钠溶液 | D. | 浓氢氧化钠溶液 |
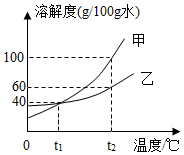 甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答.
甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答. 用侯氏制碱法制得的纯碱中常含有少量杂质,为了测定一定质量的纯碱样品所生成二氧化碳的质量,同学们设计了如图所示的实验装置.
用侯氏制碱法制得的纯碱中常含有少量杂质,为了测定一定质量的纯碱样品所生成二氧化碳的质量,同学们设计了如图所示的实验装置.