题目内容
10.工业上生产硫酸的第一步反应为:4X+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,则X为( )| A. | FeS2 | B. | Fe2S3 | C. | FeSO4 | D. | FeS |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
解答 解:根据反应的化学方程式4X+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,反应物中氧原子个数为22,反应后的生成物中铁、氧、硫原子个数分别为4、22、8,根据反应前后原子种类、数目不变,则4X中含有4个铁原子和8个硫原子,则每个X分子由1个铁原子和2个硫原子构成,则物质X的化学式为FeS2.
故选:A.
点评 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式是正确解题的关键.

练习册系列答案
相关题目
20.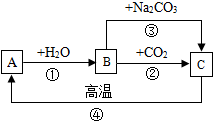 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )| A. | A物质的化学式是:CaO | |
| B. | B物质的俗称是:熟石灰或(消石灰) | |
| C. | C物质的名称是:水 | |
| D. | B物质在农业生产中的一种用途:中和酸性土壤 |
1.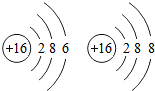 分析硫原子,硫离子的结构示意图,下列说法正确的是( )
分析硫原子,硫离子的结构示意图,下列说法正确的是( )
 分析硫原子,硫离子的结构示意图,下列说法正确的是( )
分析硫原子,硫离子的结构示意图,下列说法正确的是( )| A. | 两者电子层数相同 | B. | 两者最外层电子数相同 | ||
| C. | 两者元素种类不同 | D. | 两者质子数不同 |
15.除去下列各组物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |
2.某饮品营养成分表显示每250mL含钠78mg、钙91mg等.其中钠、钙指( )
| A. | 分子 | B. | 原子 | C. | 单质 | D. | 元素 |
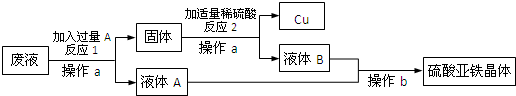
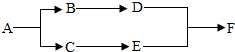 已知A、B、C、D、E、F是初中化学常见的六种物质,其中A、B是组成元素相同的两种液态物质,D是改良酸性土壤常用的碱,F是常用的建筑材料的主要成分,它们之间的转化关系如图所示:
已知A、B、C、D、E、F是初中化学常见的六种物质,其中A、B是组成元素相同的两种液态物质,D是改良酸性土壤常用的碱,F是常用的建筑材料的主要成分,它们之间的转化关系如图所示: