题目内容
钢铁是重要的金属材料,人类每年要从自然界获取大量的铁矿资源。
(1) 目前世界上已有50%以上的废钢铁得到回收利用,其目的是__________。
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(2)铁矿石的种类很多,例如磁铁矿(主要成分Fe3O4)黄铁矿(主要成分FeS2)及赤铁矿(主要成分Fe2O3)等。一般不选用 ,原因是 。
(3)工业上高炉炼铁得到的主要产品是 ;(填序号) A.纯铁 B.生铁 C.钢
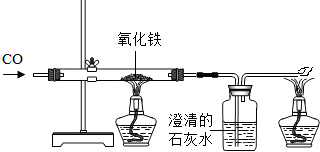
(4)小章同学准备在实验室用下图所示装置模拟工业炼铁.请你据此回答下列问题: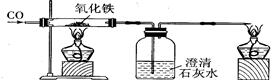
①实验中产生的现象主要有:_____________________、__________________。
②实验中发生反应的方程式为
③装置图中澄清石灰水的作用是
④某同学实验完成后,发现过量的澄清石灰水增重0.44 g,则该同学通人装置的CO气体质量__________(填“大于”、“小于”或“等于”)0.28 g,原因是 。
(1)A (2)黄铁矿 污染大,铁含量低 (3)B
(4) ①红色固体变黑 澄清石灰水变浑浊
②3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
③检验产物二氧化碳
④大于 有一部分一氧化碳没参加化学反应
解析试题分析:(1)回收利用金属是为了节约金属资源,故选A。
(2)分析①磁铁矿(主要成分:Fe3O4),②黄铁矿(主要成分:FeS2),③赤铁矿(主要成分:Fe2O3)这三种矿石,得出:②不适合用来炼铁,因为黄铁矿中铁的含量最低,同时会生成SO2等有害气体污染环境。
(3)工业上高炉炼铁得到的主要产品是生铁,故选B。
(4)用CO还原Fe2O3,生成铁和CO2气体,实验现象为由红色固体变成黑色固体,澄清石灰水变浑浊,反应方程式为3CO+Fe2O3 2Fe+3CO2;装置中的澄清石灰水是为了检验二氧化碳气体;由于CO为可燃性气体,CO还原Fe2O3的实验操作过程中,实验前要通入一段时间的CO,实验结束后继续通入CO,直至试管冷却,故CO的质量应大于0.28克。
2Fe+3CO2;装置中的澄清石灰水是为了检验二氧化碳气体;由于CO为可燃性气体,CO还原Fe2O3的实验操作过程中,实验前要通入一段时间的CO,实验结束后继续通入CO,直至试管冷却,故CO的质量应大于0.28克。
考点: 铁的冶炼原理、实验现象及操作注意事项。
点评:由于CO为可燃性气体,要使用时要注意安全。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案
 钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.
钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.