题目内容
3.某地一辆满载浓硫酸的罐车翻倒,导致溶质质量分数为98%的浓硫酸20t泄漏,并向路基两边蔓延.接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除险情.请回答:(1)溶质质量分数为98%的浓硫酸20t含H2SO4的质量是19.6t.
(2)计算中和泄漏的98%的浓硫酸20t,理论上需要氢氧化钙的质量.
(3)浓硫酸如果不慎沾在皮肤或衣服上,应立即用用干布擦掉,然后用水冲洗,然后再涂上3%-5%的小苏打溶液.
分析 (1)根据溶质的质量分数的计算公式计算;
(2)根据氢氧化钙与硫酸反应的方程式,由硫酸的质量求出氢氧化钙的质量;
(3)根据使用浓硫酸的注意事项分析回答.
解答 解:(1)98%的浓硫酸20t含H2SO4的质量是:20t×98%=19.6t.
(2)设理论上需要氢氧化钙的质量为x,
H2SO4+Ca(OH)2═CaSO4+2H2O,
98 74
19.6t x
$\frac{98}{74}=\frac{19.6t}{x}$ 解得:x=14.8t.
(3)浓硫酸不慎沾在皮肤上,应立即用干布擦掉,然后用水冲洗,最后再涂上3%~5%的小苏打溶液.
故答为:(1)19.6t;(2)理论上需要氢氧化钙的质量是14.8t.(3)小苏打.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力和使用浓硫酸的注意事项等知识,计算时要注意规范性和准确性.

练习册系列答案
相关题目
13. 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
14.某同学描述的有关实验现象如下,你认为正确的是( )
| A. | 硫在氧气中燃烧产生微弱的淡蓝色火焰,并生成有刺激性气味的气体 | |
| B. | 点燃棉制品时时产生烧焦羽毛的气味 | |
| C. | 将CO通入到灼热的氧化铜中,发现红色粉末立即变成黑色 | |
| D. | 将澄清的饱和石灰水加热,发现有白色浑浊出现 |
11.某学习小组的同学们在做氢氧化钠溶液和稀硫酸的中和反应实验中,突然发现未给烧杯中滴加指示剂.于是将实验改为探究烧杯内的溶液中溶质的成分.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想与假设】同学们经过讨论,一致认为溶质一定有硫酸钠,写出生成硫酸钠的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.溶质除了硫酸钠外,小敏同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)同学们取少量烧杯中的溶液于试管中,滴加酚酞溶液,无明显现象产生,据此推断小敏同学的猜想不成立,理由是酚酞溶液没有变红,溶液中没有氢氧化钠.
(2)小丽同学取少量烧杯中的溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,她据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl.
(3)小华同学提出质疑,因为溶液中的硫酸钠与氯化钡反应也能产生白色沉淀.为了证明溶质是否还有硫酸,请你与同学们一起进行如表探究.
【反思与评价】
(1)在探究化学反应后的剩余物质的成分是,除了考虑生成物,还要考虑反应物的用量.
(2)复分解反应发生的条件是生成物中有沉淀或有气体或有水生成.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想与假设】同学们经过讨论,一致认为溶质一定有硫酸钠,写出生成硫酸钠的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.溶质除了硫酸钠外,小敏同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)同学们取少量烧杯中的溶液于试管中,滴加酚酞溶液,无明显现象产生,据此推断小敏同学的猜想不成立,理由是酚酞溶液没有变红,溶液中没有氢氧化钠.
(2)小丽同学取少量烧杯中的溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,她据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl.
(3)小华同学提出质疑,因为溶液中的硫酸钠与氯化钡反应也能产生白色沉淀.为了证明溶质是否还有硫酸,请你与同学们一起进行如表探究.
| 实验步骤 | 实验现象 | 实验结论 |
取少量烧杯中的溶液于试管中,加入锌粒 | 有气泡产生 | 溶质还有硫酸 |
(1)在探究化学反应后的剩余物质的成分是,除了考虑生成物,还要考虑反应物的用量.
(2)复分解反应发生的条件是生成物中有沉淀或有气体或有水生成.
18.如图图象能正确反映对应的实验操作的是( )
| A. | 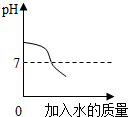 把水加到NaOH溶液中 把水加到NaOH溶液中 | |
| B. | 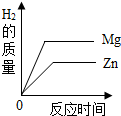 等质量的Mg和Zn与足量的稀硫酸反应,产生H2的质量 等质量的Mg和Zn与足量的稀硫酸反应,产生H2的质量 | |
| C. | 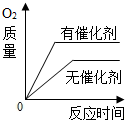 用一定量的双氧水制取氧气 用一定量的双氧水制取氧气 | |
| D. | 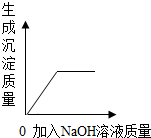 向硫酸和硫酸铜的混合溶液中滴加过量的NaOH溶液 向硫酸和硫酸铜的混合溶液中滴加过量的NaOH溶液 |
15.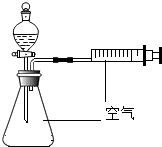 如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
滴入分液漏斗中的液体,记录注射器活塞的位置,一段时间后,可观察到注射器的活塞向左移动的是( )
 如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):| 编号 | 分液漏斗 | 锥形瓶 |
| ① | 食盐水 | 铁钉 |
| ② | H2O2水溶液 | 二氧化锰固体 |
| ③ | NaOH溶液 | FeSO4溶液 |
| ④ | 蒸馏水 | 火碱固体 |
| A. | ①② | B. | 只有① | C. | ①③ | D. | ②④ |
12.下列对某一主题知识归纳,正确的一组是
| A.生活常识 | B.物质鉴别 |
| 硬水与软水--观察颜色区别 人体缺钙元素--甲状腺肿大 | 食盐与亚硝酸钠--品尝味道 氮气与二氧化碳--燃着的木条 |
| C.安全常识 | D.“一定”与“不一定” |
| 长时间堆放的柴草--要不时翻动 进入陌生的溶洞前--先做灯火实验 | 有盐和水生成的反应一定是中和反应 浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液 |
| A. | 生活常识 | B. | 物质鉴别 | ||
| C. | 安全常识 | D. | “一定”与“不一定” |