题目内容
5.某兴趣小组的同学在实验室用含有少量氯化钙的氯化钠固体配制一定质量分数的氯化钠溶液,实验步骤如图所示: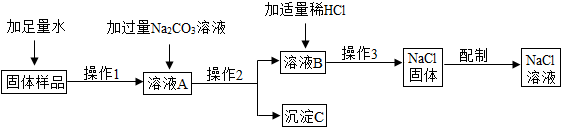 请据图回答:
请据图回答:(1)在“操作2”中,要用到的玻璃仪器除玻璃棒、烧杯外,还有漏斗.
(2)加入“适量稀HCl”的目的是除去溶液中过量的碳酸钠.
(3)生成沉淀C的化学方程式为CaCl2+Na2CO3=2NaCl+CaCO3↓.
(4)“操作3”的名称是蒸发.
(5)加入过量Na2CO3溶液的目的是使氯化钙完全反应
(6)在用量筒量取所需水的过程中,若俯视读数,而其余操作均正确,这样配得的溶液的溶质质量分数会偏高(填“偏高”、“偏低”、或“无影响”).
分析 由题目的信息可知:过滤要用到的玻璃仪器除玻璃棒、烧杯外,还有漏斗;加入“适量稀HCl”的目的是:除去溶液中过量的碳酸钠;“操作3”的名称是蒸发,即得到氯化钠固体;加入过量Na2CO3溶液的目的是:使氯化钙完全反应;在用量筒量取所需水的过程中,若俯视读数,而其余操作均正确,这样配得的溶液的溶质质量分数会偏高,因为俯视水量少了.
解答 解:(1)过滤要用到的玻璃仪器除玻璃棒、烧杯外,还有漏斗;故答案为:漏斗;
(2)加入“适量稀HCl”的目的是:除去溶液中过量的碳酸钠;故答案为:除去溶液中过量的碳酸钠;
(3)氯化钙和碳酸钠反应生成氯化钠和碳酸钙白色沉淀,配平即可;故答案为:CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)“操作3”的名称是蒸发,即得到氯化钠固体;故答案为:蒸发;
(5)加入过量Na2CO3溶液的目的是:使氯化钙完全反应;故答案为:使氯化钙完全反应;
(6)在用量筒量取所需水的过程中,若俯视读数,而其余操作均正确,这样配得的溶液的溶质质量分数会偏高,因为俯视水量少了;故答案为:偏高;
点评 实验探究题是近几年中考的重点内容之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过查阅资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握,本考点主要出现在实验题中.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
2.有三瓶无色、无味的气体x、y、z,它们分别是甲烷、氢气、一氧化碳中的一种,分别点燃三种气体,用干燥的冷烧杯罩在火焰上方,只有y和z火焰上方的烧杯内壁有水滴出现,燃烧后分别向烧杯中注入澄清的石灰水,振荡,只有x和y的烧杯内石灰水变浑浊,则x、y、z分别是( )
| A. | 一氧化碳 甲烷 氢气 | B. | 甲烷 一氧化碳 氢气 | ||
| C. | 甲烷 氢气 一氧化碳 | D. | 氢气 甲烷 一氧化碳 |
17.在天平两边托盘中的烧杯中各放入质量和质量分数相同的足量的盐酸,调节天平至平衡,分别向两边烧杯中各加入8g镁和铁,反应完全后天平的指针( )
| A. | 偏向加铁的一边 | B. | 偏向加镁的一边 | ||
| C. | 停留在原位 | D. | 不能确定偏向哪边 |
15.下列4个图象中,能正确反应变化关系的是( )
| A. | 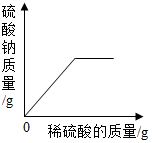 向一定质量的氢氧化钠溶液中加入稀硫酸至过量 向一定质量的氢氧化钠溶液中加入稀硫酸至过量 | |
| B. |  向一定质量的稀硫酸中加入锌片 向一定质量的稀硫酸中加入锌片 | |
| C. | 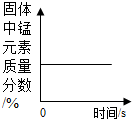 加热一定质量的高锰酸钾固体 加热一定质量的高锰酸钾固体 | |
| D. | 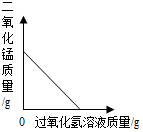 向一定质量的二氧化锰中加入过氧化氢溶液 向一定质量的二氧化锰中加入过氧化氢溶液 |

 某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.
某化学小组在课外活动时按如图所示组装好仪器,在甲试管中装入碳酸钙,乙试管装入紫色石蕊溶液.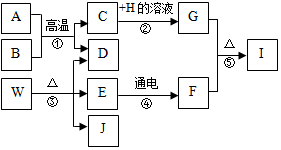 以下物质为初中化学常见物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,W绿色固体,H的溶液呈蓝色,常温下B、D、F均为无色气体且BD元素组成完全相同.(反应②、④的个别生成物已略去)
以下物质为初中化学常见物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,W绿色固体,H的溶液呈蓝色,常温下B、D、F均为无色气体且BD元素组成完全相同.(反应②、④的个别生成物已略去)