题目内容
5.200克某硫酸恰好与26克锌完全反应,试计算:(1)生成氢气的质量;
(2)硫酸溶液中溶质的质量分数;
(3)充分反应后所得溶液的质量.
分析 根据锌与硫酸反应的方程式,由锌的质量可以求出生成的氢气的质量及参加反应稀硫酸溶质的质量,再根据溶质质量分数的计算公式计算即可.
解答 解:设制得氢气的质量为x,稀硫酸中溶质的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
26g y x
$\frac{65}{26g}$=$\frac{98}{y}$=$\frac{2}{x}$
x=0.8g
y=39.2g
(1)生成氢气的质量为0.8g;
(2)硫酸溶液中溶质的质量分数为:$\frac{39.2g}{200g}$×100%=19.6%
(3)充分反应后所得溶液的质量为:200g+26g-0.8g=225.2g.
故答案为:(1)0.8g;
(2)19.6%
(3)225.2g.
点评 本题主要考查学生对物质质量分数和溶质质量分数的计算能力.学生需正确书写出化学方程式,并能正确运用溶质质量分数公式进行计算,才能正确答题.

练习册系列答案
相关题目
16.2015年5月16日,山西省阳城县某化工有限公司发生一起二硫化碳(CS2)泄漏事故.二硫化碳是一种易挥发、易燃、有毒、难溶于水的液体.下列说法正确的是( )
| A. | 二硫化碳中硫的化合价为-2价,它属于氧化物 | |
| B. | 二硫化碳的化学性质很稳定,很难发生化学反应 | |
| C. | 二硫化碳是一种重要的化学试剂,应该密封保存 | |
| D. | 二硫化碳泄露后,可用水稀释溶解除去 |
13.分子、原子等粒子构成物质,用我们所学的分子、原子的相关知识解释下列现象,正确的是( )
| A. | 墙内开花墙外香,是由于分子在不断运动 | |
| B. | 冰冻三尺非一日之寒,水结冰时,分子静止不动 | |
| C. | 空气中的氧气、二氧化碳经混合,它们的化学性质改变 | |
| D. | 经过液化、蒸发从空气中得到氮气和氧气的过程属于化学变化 |
10.下列做法中错误的是( )
| A. | 为减少白色污染,少使用塑料袋 | B. | 倡导低碳生活,多步行,少开车 | ||
| C. | 油锅着火时盖上锅盖灭火 | D. | 用氢氧化钠改良酸性土壤 |
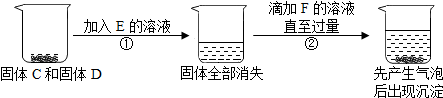
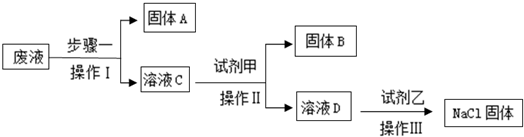
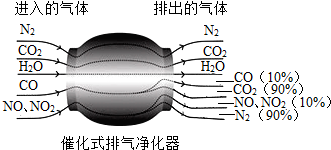 化学与生活、生产息息相关,请运用化学知识回答以下问题.
化学与生活、生产息息相关,请运用化学知识回答以下问题.