题目内容
19.取少量木炭粉和足量氧化铜充分反应,试验后的混合粉末中含有铜和氧化铜,实验室从该混合粉末中回收铜的方案如下: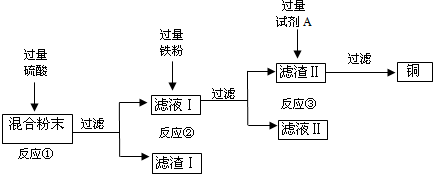
(1)写出反应①的化学方程式CuO+H2SO4═CuSO4+H2O.
(2)在进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和漏斗.过滤时,发现速度很慢,原因可能是滤纸和漏斗壁之间有气泡.
(3)反应③中产生了大量气泡,则所选用的试剂A为HCl或H2SO4溶液(填化学式).
(4)反应②中,加入过量铁粉的目的是使硫酸铜完全反应.
(5)回收反应后的铜,对于金属资源的保护意义重大,请你再写出一种保护金属资源的方法或途径寻找金属替代品.
分析 (1)反应①中,氧化铜和稀硫酸反应生成硫酸铜和水;
(2)在进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和漏斗,过滤时,如果滤纸和漏斗壁之间有气泡,会导致过滤速度减慢;
(3)铁和稀盐酸反应生成氯化亚铁和氢气,和稀硫酸反应生成硫酸亚铁和氢气;
(4)反应②中,加入过量铁粉能使硫酸铜完全反应;
(5)回收利用废旧金属,防止金属生锈,寻找金属替代品,合理开发利用金属,都能够保护金属资源.
解答 解:(1)反应①中,氧化铜和稀硫酸反应生成硫酸铜和水,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O.
故填:CuO+H2SO4═CuSO4+H2O.
(2)在进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和漏斗,过滤时,发现速度很慢,原因可能是滤纸和漏斗壁之间有气泡.
故填:漏斗;滤纸和漏斗壁之间有气泡.
(3)反应③中产生了大量气泡,则所选用的试剂A可能是稀盐酸,也可能是稀硫酸,这是因为稀盐酸、稀硫酸都能够和铁反应生成氢气.
故填:HCl或H2SO4.
(4)反应②中,加入过量铁粉的目的是使硫酸铜完全反应.
故填:使硫酸铜完全反应.
(5)保护金属资源的方法或途径有:回收利用废旧金属,防止金属生锈,寻找金属替代品,合理开发利用金属等.
故填:寻找金属替代品.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
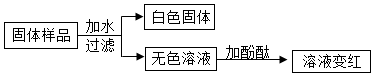
9.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 可燃物的燃烧既属于氧化反应,也属于化合反应 | |
| B. | 蔗糖的饱和溶液不能再溶解蔗糖,也一定不能再溶解其他物质 | |
| C. | 向某固体滴加稀盐酸,若有气泡产生,则该固体中一定含有碳酸根 | |
| D. | 化学反应前后由于原子种类不变,所以元素种类也不变 |
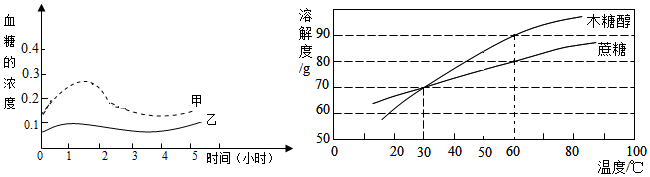
10.下列有关人体新陈代谢的说法正确的是( )
| A. | 蛋白质在体内代谢的最终产物是水和二氧化碳 | |
| B. | 淀粉在消化道内最终被氧化分解成葡萄糖 | |
| C. | 膳食纤维不能被人体消化吸收 | |
| D. | 人体的异化作用就是指人体的呼吸作用 |
7.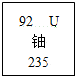 “七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )
“七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )
 “七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )
“七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )| A. | 铀是一种非金属元素 | B. | 铀原子的核外电子数为235 | ||
| C. | 铀原子的中子数为143 | D. | 铀原子的相对原子质量为112克 |
14.2016年9月,合肥市在全省率先推出“午餐工程”,学生可以选择在学校享用统一提供的午餐并休息.某校食堂提供了下列5种食物:

小亮同学为自己安排的午餐食谱中,较合理的是( )

小亮同学为自己安排的午餐食谱中,较合理的是( )
| A. | ①②③ | B. | ①③⑤ | C. | ①④⑤ | D. | ③④⑤ |
8.下列关于物质的性质和用途的表述没有直接联系的是( )
| 选项 | 性质 | 用途 |
| A | 常温下碳的化学性质不活泼 | 用墨绘制字画 |
| B | 醋酸显酸性 | 用醋酸除去热水瓶中的水垢 |
| C | NaOH能与油脂反应 | 用NaOH除去油污 |
| D | CO常温下是气体 | 用CO作燃料 |
| A. | A | B. | B | C. | C | D. | D |
9.如图所示图象能正确反映对应实验操作的是( )
| A. | 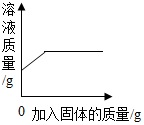 在一定量的稀盐酸中加入过量石灰石 | |
| B. | 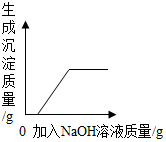 向氯化钾和硫酸铜的混合溶液中滴加氢氧化钠溶液 | |
| C. | 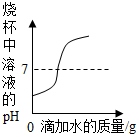 向盛有一定量稀硫酸的烧杯中不断加水稀释 | |
| D. | 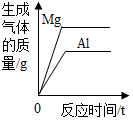 将等质量的镁粉和铝粉分别与足量等浓度的稀硫酸反应 |