题目内容
3.如图1是元素周期表的一部分和一些微粒的结构示意图,请回答下列问题.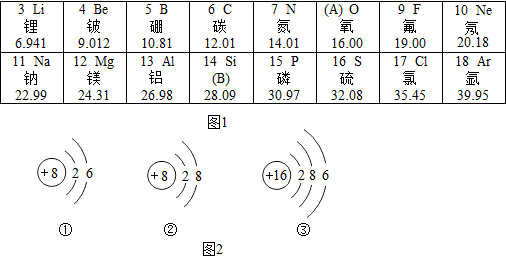
(1)图1中A、B处应分别填写8、硅.
(2)图2中表示氧原子结构示意图的是①,从该示意图中的数字6可看出氧元素的化学性质比较活泼.
(3)某物质经测定不含氧元素,则它可能属于下列物质中的ACD(填字母).
A.酸 B.碱 C.盐 D.有机物.
分析 (1)根据元素周期的信息来分析;
(2)根据原子结构示意图的意义来分析;
(3)根据物质的组成来分析.
解答 解:(1)A是氧的原子序数,为8;14号元素是硅元素,故填:8;硅;
(2)氧原子的原子序数为8,则核内有8个质子,核外电子数为8个,最外层有6个电子,在化学反应中易得到电子,化学性质活泼;故填:①;6;
(3)酸中可能不含氧元素,如盐酸;碱中一定含有氧元素;盐中可能不含氧元素,如氯化钠;有机物中可能不含氧元素,如甲烷.故填:ACD.
点评 本题考查学生熟练掌握应用元素周期表和原子结构示意图所提供的信息进行分析解题的能力.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
13.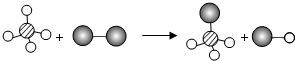 如图表示两种位置发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )
如图表示两种位置发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )
 如图表示两种位置发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )
如图表示两种位置发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法中不正确的是( )| A. | 图中有4种分子 | B. | 产物是混合物 | ||
| C. | 反应前后原子个数不变 | D. | 发生了化合反应 |
11.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行了如下探究活动.
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数
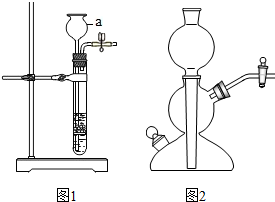
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(3)将稀盐酸滴入样品中,产生气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,反应一段时间后,当观察到无气泡产生(填实验现象),才停止滴加稀盐酸.
(4)实验结束后,量筒内进入水的体积如图2所示,其读数为165mL.已知在该实验条件下,生成气体的密度为2g•L-1,通过计算,样品中R的质量分数为25%.
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 溶液变成红色 | 该样品还含有氢氧化钙 |
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(3)将稀盐酸滴入样品中,产生气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,反应一段时间后,当观察到无气泡产生(填实验现象),才停止滴加稀盐酸.
(4)实验结束后,量筒内进入水的体积如图2所示,其读数为165mL.已知在该实验条件下,生成气体的密度为2g•L-1,通过计算,样品中R的质量分数为25%.
18.下列做法不会危害人体健康的是( )
| A. | 用甲醛溶液浸泡海产品 | B. | 将霉变大米加工成雪饼出售 | ||
| C. | 用纯碱除去鱼肉上酸性胆汁的苦味 | D. | 焚烧塑料消除“白色污染” |
15.下列变化属于化学变化的是( )
| A. | 试管破裂 | B. | 铁钉生锈 | C. | 灯泡发光 | D. | 盐酸挥发 |
12.下列物质的化学式书写正确的是( )
| A. | 干冰:H2O | B. | 熟石灰:CaO | C. | 烧碱:NaOH | D. | 纯碱:NaCO3 |
13.下列物质露置于空气中,一段时间后,因为物理变化质量增大的是( )
| A. | 熟石灰 | B. | 氧化钙 | C. | 氢氧化钠 | D. | 浓硫酸 |
 经过一年的学习,我们已经掌握了气体实验室制法的一些知识.
经过一年的学习,我们已经掌握了气体实验室制法的一些知识.