题目内容
13.将废旧的电子元件进行粗加工,可得到含有金属铝、铁、铜等的粉末,从这类粉末中可分离和制取有关金属和化工原料AICI3,实验过程如下:
请回答:
(1)操作①中得到的金属A是铁;操作a的名称是过滤;在蒸发过程中需要使用玻璃棒,其作用是搅拌,防止局部温度过高造成液滴飞溅.
(2)写出步骤②所涉及的化学反应方程式:2Al+6HCl=2AlCl3+3H2↑.
(4)实验步骤②中除了加入稀盐酸外,还可选用下列试剂a(填标号).
a.氯化铜溶液 b.氯化钠溶液 c.硝酸银溶液.
分析 (1)根据铁能够被磁铁吸引,因此A是铁;铝和铜的混合物中,加入适量的稀盐酸,铝和稀盐酸反应生成氯化铝和氢气,铜不反应,因此过滤可以得到B,即金属铜;在蒸发过程中需要使用玻璃棒,其作用是搅拌作用,是为了防止局部温度过高造成液滴飞溅进行分析;
(2)根据铝和盐酸反应生成氯化铝和氢气进行分析;
(4)根据步骤②中除了加入稀盐酸溶液外,还可选用的试剂是加入氯化铜,铝与氯化铜反应生成氯化铝和铜进行分析.
解答 解:(1)铁能够被磁铁吸引,因此A是铁;铝和铜的混合物中,加入适量的稀盐酸,铝和稀盐酸反应生成氯化铝和氢气,铜不反应,因此过滤可以得到B,即金属铜;在蒸发过程中需要使用玻璃棒,其作用是搅拌作用,是为了防止局部温度过高造成液滴飞溅;
(2)铝和盐酸反应生成氯化铝和氢气,化学方程式为:2Al+6HCl=2AlCl3+3H2↑;
(3)步骤②中除了加入稀盐酸溶液外,还可选用的试剂是加入氯化铜,铝与氯化铜反应生成氯化铝和铜,故选:a.
故答案为:(1)铁,过滤,搅拌,防止局部温度过高造成液滴飞溅;
(2)2Al+6HCl=2AlCl3+3H2↑;
(3)a.
点评 明确金属的物理性质及化学性质是解答本题关健.熟记金属活动性顺序表,氢前金属与酸反应,活动性强的金属能置换活动性弱的金属.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
1.下列有关燃烧与灭火的说法中错误的是( )
| A. | 用灯帽盖灭酒精灯--隔绝空气 | |
| B. | 森林灭火时,建立隔离带--隔绝可燃物 | |
| C. | 家具起火,用水扑灭--降低温度 | |
| D. | 煤炉生火时,用木柴引燃--提高着火点 |
8.生活中遇到的问题,常常涉及化学知识.下列说法中.不正确的是( )
| A. | 将青菜放入着火的油锅以降低其着火点 | |
| B. | 将用过的铁锅洗净擦干以防生锈 | |
| C. | 用加热煮沸的方法可降低水的硬度 | |
| D. | 用燃烧闻气味的方法可鉴别棉纤维和羊毛 |
5.下列化肥中属于氮肥的是( )
| A. | 磷矿粉 | B. | 氯化钾 | C. | 过磷酸钙 | D. | 硫酸铵 |
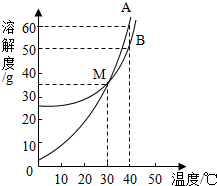 A、B两种物质的溶解度曲线如图.
A、B两种物质的溶解度曲线如图.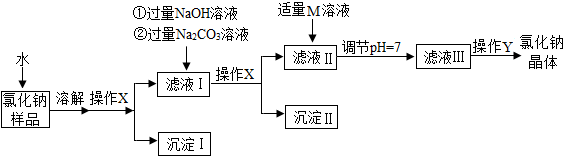
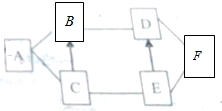 A~F都是初中化学中常见的物质,其中A是目前年产量最高的金属,B的溶液是黄色,F是造成温室效应的主要气体,它们之间的转化关系如图所示,(“-”表示相互间能反应,“→”表示在某种条件下能生成该物质),请回答下列问题:
A~F都是初中化学中常见的物质,其中A是目前年产量最高的金属,B的溶液是黄色,F是造成温室效应的主要气体,它们之间的转化关系如图所示,(“-”表示相互间能反应,“→”表示在某种条件下能生成该物质),请回答下列问题: