题目内容
17.空气是人类活动必需的自然资源,工业上常用分离空气的方法制取氧气,实验室常用物质分解的方法制取氧气.
(1)工业制氧气是物理(填“物理”或“化学”)变化.
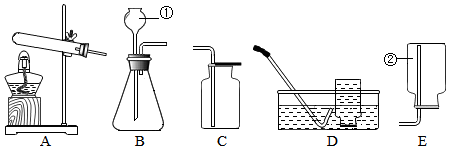
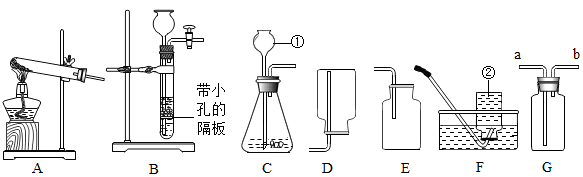
(2)图中仪器a的名称是铁架台,b的名称是锥形瓶.
(3)实验室用高锰酸钾制取氧气,可选择A作气体发生装置(填字母代号),此法制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,当用C收集氧气时,当看到集气瓶口有大量气泡冒出时表明气体已收集满.
(4)检查B装置气密性的方法是将装置中导气管上的胶皮管用弹簧夹夹住,向长颈漏斗中注水至形成一段液柱,一段时间后若液柱不下降,即可证明装置不漏气.
(5)实验室制取H2气体时,可用C或E装置收集,由此推测H2所具有的物理性质是bc(填序号)
a.密度大于空气 b.难溶于水 c.密度小于空气.
分析 (1)工业制氧气的过程中没有新物质生成,属于物理变化;
(2)根据常用仪器的名称进行分析;
(3)根据用高锰酸钾制取氧气需要加热选择气体发生装置即可;根据高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气写出反应的化学方程式即可;根据用排水法收集氧气时已收集满时的现象进行分析;
(4)根据检查装置气密性的方法进行分析;
(5)根据收集气体的方法可以判断气体的性质.
解答 解:(1)工业制氧气的过程中没有新物质生成,属于物理变化;
故填:物理;
(2)图中仪器a的名称是铁架台,b的名称是锥形瓶;
故填:铁架台;锥形瓶;
(3)实验室用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;用排水法收集氧气时,收集时观察到集气瓶口有大量气泡冒出时表明氧气已集满;
故填:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;集气瓶口有大量气泡冒出;
(4)检查B装置气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,向长颈漏斗中注水至形成一段液柱,一段时间后若液柱不下降,即可证明装置不漏气;故填:将装置中导气管上的胶皮管用弹簧夹夹住,向长颈漏斗中注水至形成一段液柱,一段时间后若液柱不下降,即可证明装置不漏气;
(5)氢气可用C装置收集,说明氢气不溶于水;氢气可用E装置收集,说明氢气的密度比空气小.
故填:bc.
点评 本题考查仪器的用途、装置的选择、化学方程式的书写,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、密度、能否和空气中的物质发生化学反应等因素.

 导学全程练创优训练系列答案
导学全程练创优训练系列答案| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | Fe+H2SO4=FeSO4+H2↑ | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2↑ | D. | Cu+2HCl=CuCl2+H2↑ |
【提出问题】:什么物质是该反应催化剂?
【查阅资料】铁与氧气、水反应生成铁锈,铁锈的主要成分为氧化铁.
【猜想与假设】
假设一:小芳同学认为生锈铁钉表面的氧化铁是H2O2溶液分解反应的催化剂.
假设二:小华同学认为生锈铁钉里的铁是H2O2溶液分解反应的催化剂.
【实验与结论】:
| 实验操作 | 实验现象 | 实验结论 |
| 实验I:把一定质量的氧化铁粉末加入到装有10mL5%的过氧化氢溶液的试管中,并用一根带火星的小木条置于试管口,观察现象. | 产生气泡,带火星的木条复燃 | 反应的文字表达式 过氧化氢$\stackrel{氧化铁}{→}$水+氧气假设一成立 |
| 实验Ⅱ:取10mL5%的过氧化氢溶液于另一支试管中,加入铁,并用一根带火星的小木条置于试管口,观察现象. | 无现象 | 假设二不成立(填“成立”或“不成立”) |
同学们讨论后认为,小芳的“实验I”还不能够确切的说明氧化铁就是过氧化氢分解制取氧
气的催化剂,理由是:没有验证氧化铁的质量和化学性质反应前后是否改变.
【反思与评价】小强通过仔细观察发现“实验Ⅱ”中一直没有现象的试管,过了一段时间后试管中也出现了气体,小强觉得很奇怪,你能猜想其中的原因吗?铁与过氧化氢溶液中的氧气和水反应生成了铁锈.
| A. |  加热液体 | B. |  倾倒液体 | C. |  点燃酒精灯 | D. |  量取液体 |
| A. | 氧(O) | B. | 硅(Si) | C. | 铝(Al) | D. | 铁(Fe) |