题目内容
2.某同学利用如右图所示的A.B.C三个装置连接成一套制取并检验二氧化碳气体的装置.试回答下列问题: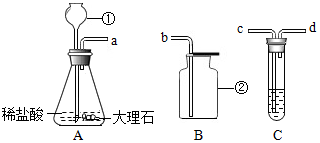
(1)图中编号仪器的名称是:①长颈漏斗,②集气瓶;
(2)装置C中的溶液是澄清石灰水(填名称);
(3)整套装置连接的正确顺序为acdb(填导管口的字母);
(4)装置A中发生反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)某化学实验小组搜集了一些小石子进行探究.取12克小石子(主要成分是碳酸钙)放入烧杯中,并加入足量的稀盐酸(杂质不参加反应).反应开始时,烧杯及所盛物质的总质量为300.0克.实验数据记录如下:
| 反应时间/min | 0 | 4 | 8 | 12 | 16 | 20 |
| 烧杯及所盛物质的总质量/克 | 300.0 | 299.0 | 296.5 | 295.6 | m | 295.6 |
②计算小石子中碳酸钙的质量分数.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室检验二氧化碳常用澄清石灰水进行分析;
(3)根据洗气应该长进短出进行分析;
(4)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(5)根据反应的化学方程式结合表格提供的数据进行分析解答即可.
解答 解:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗,②是集气瓶;
(2)实验室检验二氧化碳常用澄清石灰水;
(3)洗气应该长进短出,所以整套装置连接的正确顺序为acdb;
(4)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(5)①分析表格可以看出,第十二分钟和第二十分钟剩余物质质量相等,所以m的值为295.6;
②由质量守恒定律可知,产生二氧化碳的质量为:300g-295.6=4.4g,
设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$
x=10g
所以碳酸钙的质量分数为:$\frac{10g}{12g}$×100%≈83.3%.
故答案为:(1)长颈漏斗,集气瓶;
(2)澄清石灰水;
(3)acdb;
(4)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(5)①295.6;
②83.3%.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
18.2017年4月初,一段以“白酒加水混合假酒判定方法”的视频在网络上被大量转载,引发了行业人士关注.白酒的主要成分是乙醇(C2H5OH),下列关于乙醇的说法正确的是( )
| A. | 属于有机物 | B. | 由四种元素组成 | ||
| C. | 氧元素的质量分数最大 | D. | 完全燃烧生成水和一氧化碳 |
19.如图是氢气在氯气中燃烧的微观模拟图,有关该反应说法错误的是( )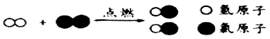
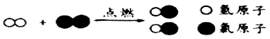
| A. | 反应生成的物质化学式是HCl | B. | 反应前后原子个数减少 | ||
| C. | 该反应为化合反应 | D. | 物质的燃烧不一定需要氧气 |
16.2016年11月10日国务院印发《控制污染物排放许可制实施方案》,其目的是改善环境质量.以下行为有利于改善环境质量的是( )
| A. | 造纸厂废水直接排放 | B. | 大力推广新能源汽车 | ||
| C. | 购物尽量使用一次性塑料袋 | D. | 生活垃圾填海 |
3.研究和学习化学,有许多重要的方法.下列方法中所举示例正确的是( )
| 选项 | 方法 | 示例 |
| A | 观察法 | 变化中观察到有发光、放热现象即可说明发生了化学变化 |
| B | 归纳法 | 水、二氧化碳是由分子构成的,归纳出所有物质都是由分子构成的 |
| C | 类比法 | 一氧化碳有毒,推测二氧化碳也有毒 |
| D | 分类法 | 根据原子最外层电子数,将元素分为金属元素、非金属元素、稀有气体元素 |
| A. | A | B. | B | C. | C | D. | D |
12.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | FeCl2溶液(CuCl2) | 加入过量的铁粉 | 过滤 |
| B | CaO(CaCO3) | 足量的水 | 溶解、过滤、干燥 |
| C | HCl(H2SO4) | 适量的Ba(NO3)2溶液 | 过滤 |
| D | Na2CO3溶液(NaCl) | 适量的AgNO3溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |

 水是生命之源.
水是生命之源.