题目内容
6.化学实验竞赛中,甲、乙两组抽到的题目是“从NaCl和Na2CO3的固体混合物中提纯NaCl,并测定碳酸钠的质量”.甲、乙两组同学的实验方案及相关数据如下.已知:Na2CO3+CaCl2=2NaCl+CaCO3↓
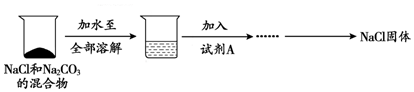
| 加入试剂A | 测得数据 | |
| 甲组方案 | 过量CaCl2溶液 | CaCO3沉淀5g |
| 乙组方案 | 适量稀硫酸 | CO2气体2.2g |
(2)老师指出甲、乙两组方案均不能得到纯净的NaCl,请选择一种方案回答下列问题.
①该方案不能得到纯净的NaCl的原因是甲方案:①引入新杂质CaCl2或乙方案:①引入新杂质Na2SO4.
②该方案的改进方法是甲方案加入适量的CaCl2
或乙方案加入适量稀盐酸.
分析 (1)根据测得的碳酸钙沉淀或产生的二氧化碳的质量计算碳酸钠的质量;
(2)根据除杂”不增、不减“的原则分析评价.
解答 解:(1)根据甲方案,生成的碳酸钙的质量为5g
设原混合物中碳酸钠的质量为x,
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{x}$=$\frac{100}{5g}$ 解得:x=5.3g
(2)由于过量的氯化钙会引入新的杂质,因此甲方案应该加入适量的氯化钙;稀硫酸和碳酸钠反应会产生新的杂质硫酸钠,因此可以将硫酸换成稀盐酸;
故答案为:(1)5.3
(2)甲方案:①引入新杂质CaCl2②加入适量的CaCl2
或乙方案:①引入新杂质Na2SO4②加入适量稀盐酸
点评 本考点属于盐的性质中实验方法和过程的探究,根据物质的溶解性和除杂质的条件,要认真分析,不仅要把握实验设计的每一个步骤中的实验目的,还要加强记忆除去常用离子的方法,从而突破难点.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
20.下列曲线示意图与相应选项表示不正确的是( )
| A. | 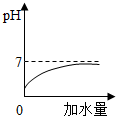 表示稀盐酸中滴加蒸馏水 | |
| B. | 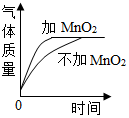 表示等体积、等质量分数的过氧化氢溶液分解 | |
| C. | 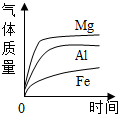 表示质量、颗粒大小都相等的金属中加稀盐酸 | |
| D. | 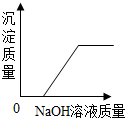 表示HCl和FeCl3的混合溶液中滴加NaOH溶液 |
1.C919的厨房为乘客提供了下列饮品:蒸馏水、雪碧、牛奶等.请从A或B两题中任选1个作答,若两题均作答,按A计分.
| A | B |
| (1)上述饮品中属于纯净物的是蒸馏水. (2)牛奶中含有丰富的“钙”,这里的“钙”指的是元素(填“单质”“元素”或“原子”). | (1)上述饮品中属于溶液的是雪碧. (2)上述饮品均能给人体提供营养素--水.水是由分子(填“元素”“分子”或“原子”)构成. |
15.下列说法正确的是( )
| A. | 洗洁精和汽油都能清洗油污,其原理不相同 | |
| B. | 酸碱中和反应生成盐和水,生成盐和水的反应不一定是中和反应 | |
| C. | 溶液结晶后溶质减少,所以饱和溶液结晶后溶质的质量分数一定减小 | |
| D. | 向久置于空气的氢氧化钠溶液中滴入酚酞试液,溶液变红,说明氢氧化钠溶液未变质 |
16.垃圾分类从我做起,金属饮料罐属于( )
| A. |  可回收物 | B. |  有害垃圾 | C. |  厨余垃圾 | D. |  其他垃圾 |


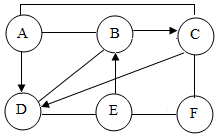 现有A、B、C、D、E、F六种初中化学常见的物质,在常温下A、B为气体单质,且B气体在同等条件下是密度最小的气体,C常用作导线的内部材料,C和D含有相同元素,E是一种溶液,溶质是由两种元素组成的化合物,用两圆间的“──”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:(以上反应均在初中知识范围内)
现有A、B、C、D、E、F六种初中化学常见的物质,在常温下A、B为气体单质,且B气体在同等条件下是密度最小的气体,C常用作导线的内部材料,C和D含有相同元素,E是一种溶液,溶质是由两种元素组成的化合物,用两圆间的“──”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:(以上反应均在初中知识范围内)