题目内容
4.图为初中化学常见气体的发生与收集装置.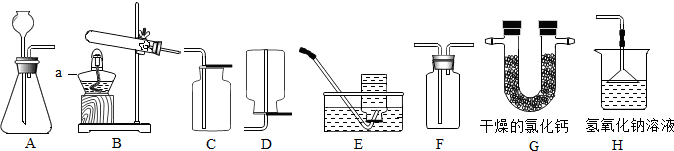
(1)用A或B装置都可以制取氧气,写出实验室制取氧气的任意一个化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,收集氧气可选用的收集装置是C或E(填装置编号,下同).
(2)用A装置也可制取二氧化碳,写出实验室制取二氧化碳的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,集满二氧化碳的集气瓶,应该正放(填“正放”或“倒置”)在实验台上.
(3)硫化氢(H2S)气体是一种有臭鸡蛋气味的有毒气体,易溶于水且水溶液呈酸性.其实验室制取原理是FeS(固)+H2SO4═FeSO4+H2S↑.要制取干燥的硫化氢气体,并处理尾气,防止污染空气,所选择的装置连接顺序依次是AGFH.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室制取硫化氢气体的原理是FeS(固)+H2SO4═FeSO4+H2S↑,因此不需要加热;硫化氢气体可以用氯化钙干燥,为防止污染空气可以用氢氧化钠溶液吸收,所选择的装置连接顺序依次是AGFH.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾制氧气就需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;C或E;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;集满二氧化碳的集气瓶,应该正放在实验台上,因为二氧化碳的密度比空气大,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;正放;
(3)实验室制取硫化氢气体的原理是FeS(固)+H2SO4═FeSO4+H2S↑,因此不需要加热;硫化氢气体可以用氯化钙干燥,为防止污染空气可以用氢氧化钠溶液吸收,所选择的装置连接顺序依次是AGFH;故答案为:AGFH;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和吸收等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | Na2CO3、HCl、MgCl2 | B. | NaOH、FeCl3、KCl | ||
| C. | Na2CO3、H2SO4、BaCl2 | D. | Ba(OH)2、H2SO4、NaNO3 |
| A. | ②④⑤①③ | B. | ②⑤④③① | C. | ②⑤④①③ | D. | ⑤②④③① |
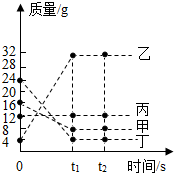 密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列不正确的是( )
密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列不正确的是( )| A. | 该反应为化合反应 | |
| B. | 该反应中,甲、乙的质量变化之比为1:4 | |
| C. | 该反应乙、丁的质量变化之比为7:5 | |
| D. | 丙可能为该反应的催化剂 |
| A. | 炊具的手柄用热固性塑料制作 | |
| B. | 新刷石灰浆的墙壁,生盆炭火干得快 | |
| C. | 不能用铁质容器盛装农药波尔多液 | |
| D. | 人体唾液的pH在0.9~1.5之间 |
| A. | 铜→氯化铜 | B. | 铁→氯化铁 | C. | 铁→硫酸亚铁 | D. | 氧化铁→氯化亚铁 |