题目内容
7.下表为元素周期表的部分信息.请回答下列问题.| ${\;}_{\;}^{1}$H | 2He | ||||||
| 3Li | 4Be | 5B | 6C | 7N | 8O | ① | 10Ne |
| ② | 12Mg | 13Ai | 14Si | 15P | 16S | ③ | 18Ar |
A.道尔顿 B.门捷列夫 C.汤姆生
(2)元素周期表中的分布是有规律的,表中①所代表的元素属于非金属元素(填“金素”或“非金属”);
(3)美国和俄罗斯的科学家,共同合成了中子数为179、相对原子质量为297的超重元素,则该元素原子的质子数为118;
(4)通过观察每一横行的元素,你能发现其中的规律是从左向右原子序数依次递增(一条即可).
分析 (1)根据化学史的知识来分析;
(2)根据元素在元素周期表中的位置确定元素的名称,然后确定元素的类别;
(3)根据相对原子质量≈质子数+中子数来分析;
(4)根据元素周期表,从原子序数等方面解答.
解答 解:(1)19世纪60年代,通过对当时发现的63种元素采用科学的分类方法,俄国化学家门捷列夫研制出世界 上第一张元素周期表;故填:B;
(2)由元素周期表的规律可知,①是氟元素,属于非金属元素;故填:非金属;
(3)因为相对原子质量≈质子数+中子数,所以该元素原子的质子数为297-179=118;故填:118;
(4)分析上表可发现:每一横行元素从左向右排列所遵循的规律是原子序数依次递增或核电荷数依次递增或质子数依次递增;故填:从左向右原子序数依次递增(答案合理即可).
点评 本题考查学生对元素周期律知识的理解,并能在解题中灵活应用的能力.

练习册系列答案
相关题目
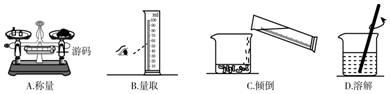
2.下列各图所示的实验操作中,正确的( )
| A. |  检查装置的气密性 | B. | 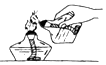 点燃酒精灯 | ||
| C. |  制取氧气 | D. |  滴加溶液 |
12.某样品为铜和氧化铜的混合物,为测定样品中氧化铜的含量,甲、乙、丙、丁四位同学用同一样品分别进行实验,测定的实验数据如下表.请分析数据解答下列问题:
(1)丙同学的实验中,样品中有8g的CuO参加了反应(填名称或化学式);
(2)四位同学中,两位同学所取的硫酸溶液质量不足(从“甲”、“乙”、“丙”或“丁”中选择填写);
(3)计算混合物氧化铜的质量分数;
(4)计算硫酸溶液中溶质的质量分数.
| 甲 | 乙 | 丙 | 丁 | |
| 所取固体样品的质量/g | 25 | 25 | 20 | 20 |
| 加入硫酸溶液的质量/g | 50 | 100 | 100 | 120 |
| 反应剩余固体的质量/g | 21 | 17 | 12 | 12 |
| 反应掉固体的质量/g | 4 | 8 | 8 |
(2)四位同学中,两位同学所取的硫酸溶液质量不足(从“甲”、“乙”、“丙”或“丁”中选择填写);
(3)计算混合物氧化铜的质量分数;
(4)计算硫酸溶液中溶质的质量分数.
19.从如图获取的信息中错误的是( )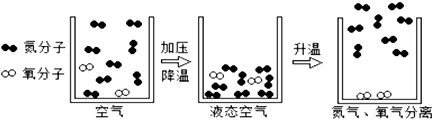

| A. | 空气是一种混合物 | B. | 氮气沸点比氧气低 | ||
| C. | 该过程为化学变化 | D. | 氧气由氧分子构成 |
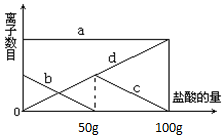 小明同学在实验室中向25g含有不溶于酸的杂质的碳酸钾配置成溶液,溶液中缓慢地滴加10%的稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡,经查询资料后得知,碳酸钾与盐酸反应先生成碳酸氢钾和氯化钾,随着盐酸的加入,碳酸氢钾再和盐酸反应生成氯化钾释放二氧化碳.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线分别与溶液中的四种离子的对应
小明同学在实验室中向25g含有不溶于酸的杂质的碳酸钾配置成溶液,溶液中缓慢地滴加10%的稀盐酸,并不断搅拌,发现开始没产生气泡,盐酸加到一定程度才产生气泡,经查询资料后得知,碳酸钾与盐酸反应先生成碳酸氢钾和氯化钾,随着盐酸的加入,碳酸氢钾再和盐酸反应生成氯化钾释放二氧化碳.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线分别与溶液中的四种离子的对应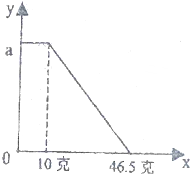 某固体物质由NaOH和MgCl2组成,取一定质量的该混合物溶于水,在所得的悬浊液中逐滴加入溶质质量分数为10%的稀盐酸,发现沉淀的质量(y)与加入盐酸的质量(x)有如图所示的关系,根据此图完成下列问题
某固体物质由NaOH和MgCl2组成,取一定质量的该混合物溶于水,在所得的悬浊液中逐滴加入溶质质量分数为10%的稀盐酸,发现沉淀的质量(y)与加入盐酸的质量(x)有如图所示的关系,根据此图完成下列问题