题目内容
10.如图是初中化学实验室制取气体的常用装置,请回答下列问题: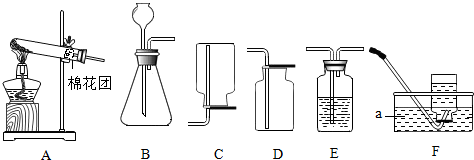
(1)标号a的仪器名称为水槽;
(2)某同学用装置A、F组合制取氧气,发生反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验结束后要先将导管移出水面,后熄灭酒精灯的原因是防止水槽里的水倒吸入试管使试管炸裂.
(3)实验室制取CO2气体时,能用装置D收集CO2气体的原因是密度比空气大,若要用E装置干燥CO2气体,E中应放入的物质名称是浓硫酸.
(4)实验室常用加热氯化铵和氢氧化钙的固体混合物来制取氨气,应选用的发生装置是A,选择的依据是反应物为固体,反应条件需要加热.
分析 (1)熟记仪器的名称;
(2)用装置A、F制取氧气,从选择合适的发生装置和收集装置看,属于“固体加热型”,排水法收集氧气(氧气不易溶于水),据此分析作答.
(3)根据二氧化碳的性质以及浓硫酸的吸水性来分析;
(4)用加热氯化铵和氢氧化钙的固体混合物来制取氨气,因为反应物为固体,反应条件需要加热,所以应选用“固固加热型”发生装置.
解答 解:(1)标号a的仪器名称为水槽;故填:水槽;
(2)用装置A、F制取氧气,从选择合适的发生装置和收集装置看,属于“固体加热型”,可用加热高锰酸钾的方法制取氧气,排水法收集氧气(氧气不易溶于水),制取氧气化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验结束后要先将导管移出水面,后熄灭酒精灯的原因是:防止水槽里的水倒吸入试管使试管炸裂;
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;防止水槽里的水倒吸入试管使试管炸裂;
(3)二氧化碳的密度比空气大,且能溶于水,所以只能用向上排空气法来收集;浓硫酸具有吸水性,所以可加入浓硫酸对气体进行干燥;故填:密度比空气大;浓硫酸;
(4)用加热氯化铵和氢氧化钙的固体混合物来制取氨气,因为反应物为固体,反应条件需要加热,所以应选用“固固加热型”发生装置,应选用的发生装置是A;理由是:反应物为固体,反应条件需要加热.故答案为:A;反应物为固体,反应条件需要加热.
点评 本题主要考查了常用气体的发生装置和收集装置与选取方法,实验室制取氧气和二氧化碳的反应原理和实验装置要掌握,这是两个比较典型的实验,具有代表性,常用的化学方程式要牢记.

练习册系列答案
相关题目
18.在硝酸根、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色.有关判断正确的是( )
| A. | 滤渣中一定有银,没有铜和锌 | |
| B. | 滤渣中一定有银和锌,可能有铜 | |
| C. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| D. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 |
15. 做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质有Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质有Na2SO4和NaOH两种物质.
(4)丁同学认为溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质.
通过进一步讨论,大家一致认为以上丁(填甲、乙、丙、丁)同学的猜想肯定错,无需实验验证.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和另外一种物质.
【实验验证】
【总结反思】戊同学根据所学化学知识和乙、丙两同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,戊同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】
(1)生活中能否用铝制品来盛放强碱性溶液?不能(选填“能”或“不能”)
(2)乙同学的实验中铝片与H2SO4溶液发生了反应,请写出铝与该溶液发生反应的化学方程式
2Al+3H2SO4═Al2(SO4)3+3H2↑.
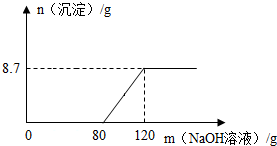
(3)镁和铝在元素周期表中处于相邻位置,向盛有100g稀硫酸的烧杯中加入一定量的Mg粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
①计算该NaOH溶液溶质的质量分数.(要求写出计算过程)
②计算该100g稀硫酸中所含溶质硫酸的质量.(要求写出计算过程)
 做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质有Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质有Na2SO4和NaOH两种物质.
(4)丁同学认为溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质.
通过进一步讨论,大家一致认为以上丁(填甲、乙、丙、丁)同学的猜想肯定错,无需实验验证.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和另外一种物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管内的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管内滴加几滴无色酚酞试液 | 无色溶液变成红色 | 猜想(3)成立 |
【知识拓展】
(1)生活中能否用铝制品来盛放强碱性溶液?不能(选填“能”或“不能”)
(2)乙同学的实验中铝片与H2SO4溶液发生了反应,请写出铝与该溶液发生反应的化学方程式
2Al+3H2SO4═Al2(SO4)3+3H2↑.
(3)镁和铝在元素周期表中处于相邻位置,向盛有100g稀硫酸的烧杯中加入一定量的Mg粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
①计算该NaOH溶液溶质的质量分数.(要求写出计算过程)
②计算该100g稀硫酸中所含溶质硫酸的质量.(要求写出计算过程)
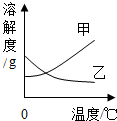
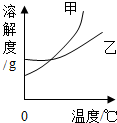
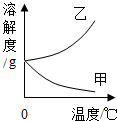
 在20℃和40℃时,分别向100g水中加入相同质量的甲和乙,充分溶解后的现象如图所示.下列图象中能正确表示甲、乙的溶解度随温度变化趋势的是( )
在20℃和40℃时,分别向100g水中加入相同质量的甲和乙,充分溶解后的现象如图所示.下列图象中能正确表示甲、乙的溶解度随温度变化趋势的是( )

 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)请回答下列问题:
”表示氢原子)请回答下列问题: