题目内容
 钙元素对人类生命和生活具有重要意义.
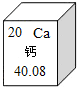
钙元素对人类生命和生活具有重要意义.(1)在元素周期表中,钙元素的信息如图所示.钙元素的相对原子质量为
(2)氧化钙能与水反应,此反应可用于
A.吸收水分 B.制熟石灰 C.加热食物
(3)能用于改良酸性土壤的含钙化合物化学式为
(4)“冰洲石”(主要成分为CaCO3)制成的工艺品不能与盐酸接触,用化学方程式表示其原因:
(5)自然界中石灰岩逐渐变成碳酸氢钙【Ca(HCO3)2】形成溶洞,碳酸氢钙是由
考点:元素周期表的特点及其应用,生石灰的性质与用途,常见碱的特性和用途,有关元素化合价的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算,化学用语和质量守恒定律,常见的碱 碱的通性
分析:(1)元素周期表中的每一个单元格的最下方的数字表示相对原子质量,可以据此解答;
(2)氧化钙和水反应放出大量的热,可以据此解答;
(3)根据化合物正负化合价的代数和为零,可以判断碘元素的化合价;
(4)碳酸钙可以和盐酸反应生成二氧化碳气体、水和氯化钙,可以据此写出该反应的化学方程式.
(5)根据碳酸氢钙的化学式解答;
(2)氧化钙和水反应放出大量的热,可以据此解答;
(3)根据化合物正负化合价的代数和为零,可以判断碘元素的化合价;
(4)碳酸钙可以和盐酸反应生成二氧化碳气体、水和氯化钙,可以据此写出该反应的化学方程式.
(5)根据碳酸氢钙的化学式解答;
解答:解:
(1)元素周期表中的每一个单元格的构成及其含义都是一样的,其中最下方的数字表示相对原子质量,所以可以得出钙元素的相对原子质量为40.08;
(2)氧化钙和水反应放出大量的热,收集其产生的热量能够给食物进行加热,该反应可以用于制取熟石灰,同样可以作为干燥剂来吸收水分;
(3)根据化合物正负化合价的代数和为零,钙显+2价,氧显-2价,可以设碘元素的化合价为x,则:+2+[x+(-2)×3]×2=0,解得:x=+5;
(4)碳酸钙可以和盐酸反应生成二氧化碳气体、水和氯化钙,可以据此写出该反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)碳酸氢钙化学式Ca(HCO3)2可知有碳氢钙氧四种元素组成;由于氢元素的相对原子质量最小,故是氢元素的质量分数最小;
0.1mol的碳酸氢钙质量:162g/mol×0.1mol=16.2g,含有氧元素的质量:16.2g×
×100%=9.6g.
答案为:(1)40.08;(2)ABC;(3)+5价;(4)CaCO3+2HCl═CaCl2+H2O+CO2↑.(5)4,H,9.6g.
(1)元素周期表中的每一个单元格的构成及其含义都是一样的,其中最下方的数字表示相对原子质量,所以可以得出钙元素的相对原子质量为40.08;
(2)氧化钙和水反应放出大量的热,收集其产生的热量能够给食物进行加热,该反应可以用于制取熟石灰,同样可以作为干燥剂来吸收水分;
(3)根据化合物正负化合价的代数和为零,钙显+2价,氧显-2价,可以设碘元素的化合价为x,则:+2+[x+(-2)×3]×2=0,解得:x=+5;
(4)碳酸钙可以和盐酸反应生成二氧化碳气体、水和氯化钙,可以据此写出该反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)碳酸氢钙化学式Ca(HCO3)2可知有碳氢钙氧四种元素组成;由于氢元素的相对原子质量最小,故是氢元素的质量分数最小;
0.1mol的碳酸氢钙质量:162g/mol×0.1mol=16.2g,含有氧元素的质量:16.2g×
| 16×3×2 |
| 162 |
答案为:(1)40.08;(2)ABC;(3)+5价;(4)CaCO3+2HCl═CaCl2+H2O+CO2↑.(5)4,H,9.6g.
点评:解答这类题目时,首先,要熟记和理解生石灰的性质与用途,还有,水的化学性质、氢氧化钙的化学性质、有关实验现象和结论(包括反应化学方程式)等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,按照题目的要求进行解答.

练习册系列答案
相关题目
2012年6月17日中国青年报报道,广东3万居民用污臭自来水近20年,广大网友提出可投入活性炭等处理受污染的自来水,活性炭的作用是( )
| A、去除异味 | B、消毒杀菌 |
| C、沉降杂质 | D、降低水的硬度 |


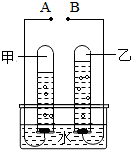 如图是电解水的实验装置图,请根据你所了解的知识填空
如图是电解水的实验装置图,请根据你所了解的知识填空 A、B、C三种物质的溶解度曲线如图所示,据图回答:
A、B、C三种物质的溶解度曲线如图所示,据图回答: