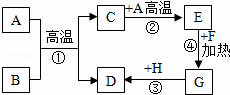
题目内容
某学习小组的同学欲探究某固体混合物A的成分,已知A中可能含有NH4Cl、CuCl2、Na2SO4、Ba(NO3)2四种物质中的两种或多种. 按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的
的反应都怡好完全反应).
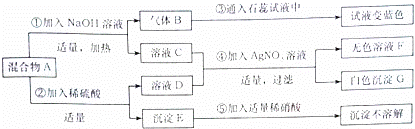
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)在常温下,气体B的水溶液pH 7 (填“大于”“小于”“等于”之一).
(2)写出1个步骤④中生成沉淀G的化学方程式: .
(3)无色溶液F中,肯定存在的酸根离子是 ,该溶液中共存在 种溶质.
(3)固体混合物A中,肯定存在的物质是 (写化学式),上述物质肯定存在的理由是 .
| 物质的鉴别、推断;溶液的酸碱性与pH值的关系;盐的化学性质;铵态氮肥的检验;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 混合物组成的推断题. |
| 分析: | 根据题中所给的各种物质都溶于水,氯化铜在溶液中显蓝色,铵态氮肥和碱混合会生成氨气,氨气的水溶液显碱性,氯离子和银离子会生成白色的氯化银沉淀,硫酸根离子和钡离子会生成白色的硫酸钡沉淀,硫酸钡沉淀、氯化银沉淀不溶于酸等知识进行分析. |
| 解答: | 解:题中所给的各种物质都溶于水,氯化铜在溶液中显蓝色,铵态氮肥和碱混合会生成氨气,氨气的水溶液显碱性,氯离子和银离子会生成白色的氯化银沉淀,硫酸根离子和钡离子会生成白色的硫酸钡沉淀,硫酸钡沉淀、氯化银沉淀不溶于酸,在混合物A中加入氢氧化钠溶液,得到气体B和溶液C,所以混合物A中一定不含氯化铜,一定含有氯化铵,氯化铵和氢氧化钠反应生成氨气,氨气溶于水形成氨水,氨水显碱性,所以溶液C中含有氯化钠,混合物A中加入稀硫酸,得到溶液D和沉淀E,所以混合物A中含有硝酸钡,硝酸钡和硫酸反应会生成白色的硫酸钡沉淀和和硝酸,氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠. (1)通过推导可知,生成的气体B是氨气,氨气溶于水形成氨水,所以在常温下,气体B的水溶液pH大于7; (2)通过推导可知,溶液B中含有氯化钠,氯化钠和硝酸银反应会生成氯化银沉淀和硝酸钠,化学方程式为:NaCl+AgNO3=NaNO3+AgCl↓; (3)氯化铵和氢氧化钠反应生成氨气、水、氯化钠、氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,溶液F中含有硝酸钠,通过推导可知混合物A中含有硝酸钡,硝酸钡和硫酸反应会生成硫酸钡沉淀和硝酸,硫酸钠和硝酸钡也会生成硫酸钡沉淀和硝酸钠,不能判断混合物A中是否含有硫酸钠,所以F中含有硝酸,所以无色溶液F中,肯定存在的酸根离子是硝酸根离子,该溶液中共存在2种溶质; (3)在混合物A中加入氢氧化钠溶液,得到气体B和溶液C,所以混合物A中一定不含氯化铜,一定含有氯化铵,氯化铵和氢氧化钠反应生成氨气,氨气溶于水形成氨水,氨水显碱性,所以溶液C中含有氯化钠,混合物A中加入稀硫酸,得到溶液D和沉淀E,所以混合物A中含有硝酸钡,所以固体混合物A中,肯定存在的物质是NH4Cl、Ba(NO3)2,肯定存在的理由是氢氧化钠和混合物A反应生成的气体通入石蕊中变蓝色,加入硫酸会生成不溶于硝酸的白色沉淀E. 故答案为:(1)大于; (2)NaCl+AgNO3=NaNO3+AgCl↓; (3)硝酸根离子,2; (4)NH4Cl、Ba(NO3)2,氢氧化钠和混合物A反应生成的气体通入石蕊中变蓝色,加入硫酸会生成不溶于硝酸的白色沉淀E. |
| 点评: | 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可. |

20世纪60年代,就有人预言可能存在由4个氧原子构成的氧分子(O4),但一直没有得到证实.最近,意大利的科学家使用普通氧分子和带正电的氧离子制造出了这种新型氧分子,并用质谱仪探测到了它的存在.下列叙述中正确的是( )
|
| A. | O4是一种新型的化合物 | B. | 一个O4分子中含有2个O2分子 |
|
| C. | O4和O2的性质完全相同 | D. | O4和O2混合后形成的是混合物 |
除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是
| 序号 | 物质 | 杂质(少量) | 试剂和操作方法 |
| A | O2 | H2O蒸汽 | 通过浓硫酸 |
| B | NaCl溶液 | Na2CO3 | 滴加适量的盐酸溶液至不再产生气泡 |
| C | NaCl固体 | 泥沙 | 加水溶解、过滤、蒸发结晶 |
| D | CO2 | HCl | 适量的NaOH溶液 |
 学式填写在下列横线上.
学式填写在下列横线上. 的一种氧化物 ;(4)常用作化肥的一种盐 .
的一种氧化物 ;(4)常用作化肥的一种盐 .