题目内容
13.日常生活中时刻发生着变化,下列变化中包含化学变化的是( )| A. | 美酒飘香 | B. | 鸡蛋变臭 | C. | 切割玻璃 | D. | 滴水成冰 |
分析 化学变化中产生了新的物质,而和物理变化没产生新的物质,所以在判断一种变化过程是何种变化时,只有抓住化学变化和物理变化的区别,即有无新物质生成来进行细心地分析、判断即可.
解答 解:A、美酒飘香是构成酒精的分子在不断运动的结果,并没有产生新的物质,故A错;
B、鸡蛋变臭有具有臭味的新物质生成,属于化学变化,故B正确;
C、切割玻璃只是将玻璃分开,并没有新物质生成,属于物理变化,故C错;
D、滴水成冰是由液态变为固态,只是状态的改变,属于物理变化,故D错.
故选B.
点评 对于化学变化和物理变化的本质区别中新物质来说,关键是个“新”字.并且,这里的“新”是相对的,而不是指自然界中原来没有的物质才算是新物质,只要是相对于变化前的物质是新的(即和变化前的物质不是同种物质),就认为是有新物质生成.

练习册系列答案
相关题目
3. 现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
【猜想假设】猜想一:没有变质,为NaOH溶液;猜想二:全部变质,为Na2CO3溶液.
猜想三:该溶液部分变质,为NaOH、Na2CO3溶液.
【查阅资料】Na2CO3溶液呈碱性,CaCl2溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案.
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
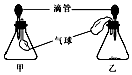
【拓展延伸】同学们设计了如图两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或
放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)若甲中充入的气体是CO2,则可能发生反应的方程式CO2+2NaOH═Na2CO3+H2O.(任写一个)
(2)若乙中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.(任写一种)
 现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.
现有一瓶无瓶盖的NaOH溶液.为确定其是否变质,同学们开始了以下探究.【猜想假设】猜想一:没有变质,为NaOH溶液;猜想二:全部变质,为Na2CO3溶液.
猜想三:该溶液部分变质,为NaOH、Na2CO3溶液.
【查阅资料】Na2CO3溶液呈碱性,CaCl2溶液呈中性.
【设计方案】请你完善下表几组同学探讨的设计方案.
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 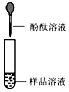 | 溶液变红,则猜想一成立. | 第2组同学认为:此方案结论不正确,理由 是:碳酸钠溶液显碱性,也能使酚酞试液变红色. |
| 第2组 | 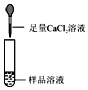 | 产生白色沉淀,反应方程式是:Na2CO3+CaCl2═2NaCl+CaCO3↓, 则猜想一不成立. | 第3组同学认为:此方 案还不能确定猜想二还是猜想三成立. |
| 第3组 |  | 滤液变红,则猜想三成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:第2组实验结束后,试管静置一段时间,取上层清液滴加酚酞溶液. |
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了如图两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或
放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
(1)若甲中充入的气体是CO2,则可能发生反应的方程式CO2+2NaOH═Na2CO3+H2O.(任写一个)
(2)若乙中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.(任写一种)
4.下列物质的俗称和化学式相一致的是( )
| A. | 纯碱--NaOH | B. | 生石灰--CaO | C. | 水银--Ag | D. | 石灰水--Ca(OH)2 |
1.为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
【探究活动二】测定样品中含有的变质固体(以下用R表示)的质量分数:
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.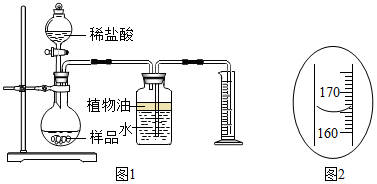
(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).
【探究活动一】检验硬化的氢氧化钙样品是否完全变质
(1)检验氢氧化钙样品是否完全变质,进行如下实验,请将实验步骤和现象补充完整:
| 实验步骤和现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,滴加酚酞试液,酚酞试液变红色 | 该样品还含有氢氧化钙 |
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中R的质量分数.实验装置(气密性良好)如图1所示.

(2)实验中量筒的作用是收集排出的水,从而确定反应生成二氧化碳的体积.
(3)实验结束后,量筒内进入水的体积如图2所示.已知在该实验条件下,生成气体的密度为2克/升,通过计算,样品中R的质量分数为25%.
(4)上述图1所示实验装置和相关试剂,用来实验测定样品中R的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:稀盐酸进入烧瓶导致计算的二氧化碳体积偏大(写一个).
18.维生素是人体必需的营养物质,维生素D2的化学式为C28H44O.下列说法正确的是( )
| A. | 维生素D2属于有机化合物 | B. | 维生素D2中含有73个原子 | ||
| C. | 维生素D2的相对分子质量是396g | D. | 维生素D2中氢元素的质量分数最大 |
1.如图为利用炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉制备黄铜(铜和锌的合金)的生产流程.下列说法正确的是( )
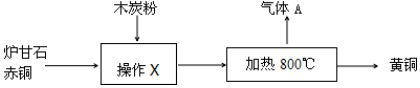

| A. | 操作X的名称是溶解 | |
| B. | 加热过程中发生的反应一定不是化合反应 | |
| C. | 气体A可能是混合物 | |
| D. | 向黄铜中加入稀盐酸,会产生气泡 |