题目内容
18.标出下列画线部分的化合价.K$\underset{Mn}{-}$O4 $\underset{Mn}{-}$O42- $\underset{N}{-}$H4+ Na$\underset{N}{-}$O2 H$\underset{N}{-}$O3 $\underset{N}{-}$H4$\underset{N}{-}$O3.
分析 根据“根”中各元素化合价代数和为“根”的化合价、在化合物中正负化合价代数和为零,结合物质的化学式进行分析解答本题.
解答 解:钾元素显+1价,氧显-2价,设高锰酸钾中锰元素的化合价为x:(+1)+x+(-2)×4=0,解得x=+7;
氧元素显-2价,设锰酸根中锰元素的化合价为y:y+(-2)×4=-2,解得y=+6;
氢元素显+1价,设铵根中氮元素的化合价为z:z+(+1)×4=+1,解得z=-3;
钠元素显+1价,氧显-2价,设亚硝酸钠中氮元素的化合价为a:(+1)+a+(-2)×2=0,解得a=+3;
氢元素显+1价,氧显-2价,设硝酸中氮元素的化合价为b:(+1)+b+(-2)×3=0,解得b=+5;
NH4NO3中铵根的元素化合价为+1.氢元素显+1价,设铵根中氮元素的化合价为c:c+(+1)×4=+1,解得c=-3;
NH4NO3中硝酸根的化合价为-1.设硝酸根中氮元素的化合价为d.d+(-2)×3=-1,解得d=+5.
故选答案为:+7;+6;-3;+3;+5;-3;+5
点评 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.

练习册系列答案
相关题目
8.生活离不开化学,下列选项中正确的是( )
| A. | 用柠檬酸、果汁、白糖、水、小苏打等可以制得汽水 | |
| B. | 人体中含量较多的前四种元素是氧、碳、氢、氮 | |
| C. | 为了节约粮食,把霉变大米淘洗后食用 | |
| D. | 食用甲醛浸泡过的海产品,可提高人体免疫力 |
9.一种石灰石样品的成分是CaCO3和SiO2,为了测定该样品中CaCO3的质量分数,现将100g稀盐酸等分5次加到35g此样品中(SiO2不溶于水也不与酸反应),得到如下数据.
(1)第3次加人盐酸后,a为25g.
(2)计算所用稀盐酸的溶质质量分数(写出计算过程).
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | 25 | a | 15 | 15 |
(2)计算所用稀盐酸的溶质质量分数(写出计算过程).
13.如表中分别列出了四种碳氢化合物的名称、相对分子质量和沸点.
(1)根据表中的信息,得知这类碳氢化合物的沸点与它的相对分子质量的关系是常温下气态物质的相对分子质量越大,沸点越高.
(2)甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中碳原子和氢原子的结合有一定规律,若分子中的碳原子数为n,则其化学式为CnH(2n+2).
| 名称 | 甲烷 | 乙烷 | 丙烷 | 丁烷 |
| 相对分子质量 | 16 | 30 | 44 | 58 |
| 沸点(℃) | -164 | -88.6 | -42.1 | -0.5 |
(2)甲烷、乙烷、丙烷、丁烷的化学式分别为CH4、C2H6、C3H8、C4H10,从中发现这类碳氢化合物的分子中碳原子和氢原子的结合有一定规律,若分子中的碳原子数为n,则其化学式为CnH(2n+2).
9.水是重要资源,我们应当认识水、用好水.下列关于水的说法中不正确的是( )
| A. | 水是食物中的重要营养素 | B. | 可以用过滤法除去水中的不溶物 | ||
| C. | 使用无磷洗衣粉有利于保护水资源 | D. | 水灭火时降低了可燃物的着火点 |
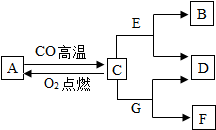 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系,请回答下列问题.
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系,请回答下列问题.