题目内容
 试验台上现有下列药品:铁粉、铁片、铜粉、铜片、5%盐酸、10%盐酸、硝酸银溶液(各种金属片已打磨,且形状、大小相同).所需仪器均已具备.
试验台上现有下列药品:铁粉、铁片、铜粉、铜片、5%盐酸、10%盐酸、硝酸银溶液(各种金属片已打磨,且形状、大小相同).所需仪器均已具备.(1)设计实验,利用上述药品验证铁、铜、银的金属活动性顺序.(要求写出实验操作,现象和结论)
(2)通过上述药品还可以探究影响化学反应速率的因素:
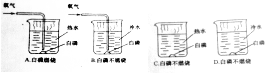
①进行如图所示实验,实验现象是
②利用上述药品,设计实验探究影响化学反应速率的另一点因素.(要求写出实验操作、现象和结论)
考点:金属活动性顺序及其应用
专题:金属与金属材料
分析:要探究金属的活动性顺序,就要选择相应的试剂,可以选择的药品是:铁片、铜片、10%盐酸、硝酸银溶液,把铁片和铜片分别插入10%盐酸中,有气泡冒出的是铁片,无变化的是铜片,说明铁比铜活泼;再把铜片插入硝酸银溶液中,铜的表面析出银白色的银,因此铜比银活泼,即铁>铜>银;进行如图所示实验,实验现象是:10%盐酸中冒出的气泡比5%盐酸冒出的气泡快,得到的结论是:盐酸的质量分数越大,反应的速度越快;影响化学反应速率的另一点因素是:药品与盐酸的接触面积越大,反应的速度越快;设计实验:把铁粉、铁片分别加入5%盐酸中,反应快的是铁粉,反应慢的是铁片;因此药品与盐酸的接触面积越大,反应的速度越快.
解答:解:(1)可以选择的药品是:铁片、铜片、10%盐酸、硝酸银溶液,把铁片和铜片分别插入10%盐酸中,有气泡冒出的是铁片,无变化的是铜片,说明铁比铜活泼;再把铜片插入硝酸银溶液中,铜的表面析出银白色的银,因此铜比银活泼,即铁>铜>银;故答案为:把铁片和铜片分别插入10%盐酸中,有气泡冒出的是铁片,无变化的是铜片,说明铁比铜活泼;再把铜片插入硝酸银溶液中,铜的表面析出银白色的银,因此铜比银活泼,即铁>铜>银;
(2)进行如图所示实验,实验现象是:10%盐酸中冒出的气泡比5%盐酸冒出的气泡快,得到的结论是:盐酸的质量分数越大,反应的速度越快;影响化学反应速率的另一点因素是:药品与盐酸的接触面积越大,反应的速度越快;设计实验:把铁粉、铁片分别加入5%盐酸中,反应快的是铁粉,反应慢的是铁片;因此药品与盐酸的接触面积越大,反应的速度越快;故答案为:①10%盐酸中冒出的气泡比5%盐酸冒出的气泡快;盐酸的质量分数越大,反应的速度越快;②设计实验:把铁粉、铁片分别加入5%盐酸中,反应快的是铁粉,反应慢的是铁片;因此药品与盐酸的接触面积越大,反应的速度越快;
(2)进行如图所示实验,实验现象是:10%盐酸中冒出的气泡比5%盐酸冒出的气泡快,得到的结论是:盐酸的质量分数越大,反应的速度越快;影响化学反应速率的另一点因素是:药品与盐酸的接触面积越大,反应的速度越快;设计实验:把铁粉、铁片分别加入5%盐酸中,反应快的是铁粉,反应慢的是铁片;因此药品与盐酸的接触面积越大,反应的速度越快;故答案为:①10%盐酸中冒出的气泡比5%盐酸冒出的气泡快;盐酸的质量分数越大,反应的速度越快;②设计实验:把铁粉、铁片分别加入5%盐酸中,反应快的是铁粉,反应慢的是铁片;因此药品与盐酸的接触面积越大,反应的速度越快;
点评:金属的活动性顺序是中考的重点内容之一,本题既考查了实验现象的描述、化学方程式的书写,又考查了学生的实验设计能力,综合性比较强.经常出现在选择题、填空题和实验题中,同学们要认真掌握.

练习册系列答案
相关题目
在下面的变化中,只有一个变化与其他的本质是不同的,该变化是( )
| A、钢铁生锈 | B、纸张燃烧 |
| C、牛奶变酸 | D、水蒸发 |
某种固体受热产生了气体,这种变化( )
| A、一定是物理变化 |
| B、一定是化学变化 |
| C、可能是物理变化,也可能是化学变化 |
| D、不是物理变化,也不是化学变化 |
鉴别氢气、一氧化碳和甲烷可以根据( )
| A、颜色 | B、溶解性 |
| C、可燃性 | D、燃烧后产物 |
在今年的化学活动周中,某校兴趣小组同学在(培养中学生基本科学素养的化学实验教学研究)课题组老师的指导下,将课本“测定空气中氧气的含量”实验装置(如甲图)改进为新的实验装置(如乙图),改进后的实验装置相当于原装置,以下评价不恰当的是( )

| A、反应容器体积小,药品消耗少 |
| B、不会因为燃烧的白磷伸入太慢导致测量误差 |
| C、装置漏气对结果无影响 |
| D、容器内径相等,易准确推算出空气中氧气的含量 |