题目内容
8.下列关于铁、铝、铜的说法正确的是( )| A. | 都是银白色的金属 | B. | 都能与稀硫酸反应 | ||
| C. | 都能被磁铁吸引 | D. | 都能与氧气反应 |
分析 A、根据铁、铝、铜三种金属的颜色,进行分析判断.
B、根据位于氢前面的金属能置换出酸中的氢,进行分析判断.
C、根据金属的特性,进行分析判断.
D、根据金属的化学性质,进行分析判断.
解答 解:A、铁、铝都是银白色的金属,但铜是紫红色金属,故选项说法错误.
B、铁、铝的金属活动性比氢强,能与稀硫酸反应;铜的金属活动性比氢弱,不能与稀硫酸反应,故选项说法错误.
C、铁能被磁铁吸引,铝、铜不能被磁铁吸引,故选项说法错误.
D、铁、铝、铜在一定条件下,均能与氧气反应,故选项说法正确.
故选:D.
点评 本题难度不大,掌握金属的化学性质(与氧气反应,活泼金属能与酸反应)、物理性质等是正确解答本题的关键.

练习册系列答案
相关题目
18.推理是学习化学的重要方法,下列推理正确的是( )
| A. | 单质中只含有一种元素,因此只含一种元素的物质一定是单质 | |
| B. | 燃烧需要同时具备三个条件,因此灭火只需要破坏其中一个即可 | |
| C. | 同种元素的原子具有相同的质子数,因此质子数相同的微粒一定属于同种元素 | |
| D. | 木炭、硫磺、红磷和铁丝燃烧都是化合反应,因此物质的燃烧一定属于化合反应 |
19.某石灰水中含有氢氧化钙1.48g,要使石灰水中含有氢氧化钙全部转化为碳酸钙沉淀,生成的沉淀质量是多少?标准状况下需要通入二氧化碳气体体积是多少升?(标准状况下二氧化碳气体的密度是1.96g/L)
16.室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为24%),另一瓶为5%的溶液,下列实验操作中,无法区分这两种溶液的是( )
| A. | 加一定量的水 | B. | 加入少量硝酸钾晶体 | ||
| C. | 略降低温度 | D. | 室温时,蒸发少量水 |
3.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
13.下列属于纯净物的是( )
| A. | 加碘食盐 | B. | 干冰 | C. | 硬水 | D. | 牛奶 |
17.下列反应不属于化学基本反应类型的是( )
| A. | NH4HCO3$\frac{\underline{\;△\;}}{\;}$NH3↑+CO2↑+H2O | B. | Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑ | ||
| C. | CaCO3+CO2+H2O=Ca(HCO3)2 | D. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C |

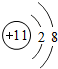 ,Y原子
,Y原子 ,Z元素的离子
,Z元素的离子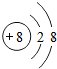 .若将0.62克X2Z放入18.2克水中得A溶液,则溶液中溶质的质量分数为4.3%,pH值>7(填“>”,“<”,“=”).
.若将0.62克X2Z放入18.2克水中得A溶液,则溶液中溶质的质量分数为4.3%,pH值>7(填“>”,“<”,“=”).