题目内容
14.在一密闭容器内有四种物质,在一定条件下发生充分反应,测得反应前后各物质的质量如表:| 甲 | 乙 | 丙 | 丁 | |
| 反应前的质量/g | 4 | 10 | 1 | 25 |
| 反应至t时刻的质量/g | 2 | a | b | 17 |
| 反应后的质量/g | 0 | 22 | 9 | d |
| A. | d的数值为9 | B. | b的数值为4 | ||
| C. | 甲和丁为反应物 | D. | 丁的相对分子质量为甲的2倍 |
分析 据质量守恒定律,再利用反应物质量会减小生成物质量会增加,催化剂质量不变,以及反应类型的特点解决此题.
解答 解:从图示的表格看:乙 和 丙的质量增加属于生成物,且分别生成 22g-10=12 g和9g-1=8g;甲的质量减少,属于反应物,且有4克物质参加反应;根据质量守恒定律可以知道丁也为反应物,且有 12g+8g-4g=16g参加反应,所以d值为 25-16=9,故该反应是甲+丁→乙+丙;
A、d的数值为9,正确;
B、根据反应中物质的质量比,设当甲反应2g,消耗丙为x
甲+丁→乙+丙;
4g 8g
2g x
$\frac{4g}{2g}=\frac{8g}{x}$
x=4g
所以b的值为1+4=5,故错误;
C、乙 和 丙的质量增加属于生成物,且分别生成 22g-10=12 g和9g-1=8g;甲的质量减少,属于反应物,且有4克物质参加反应;根据质量守恒定律可以知道丁也为反应物,故正确;
D、设甲、丁的相对分子质量为y,z.已知该反应的方程式中甲与丁的化学计量数的比为1:2,
甲~2乙
y 2z
4g 16g
$\frac{y}{4g}=\frac{2z}{16g}$
2y=z,所以丁的相对分子质量为甲的2倍,正确;
故选:B.
点评 本题主要考查质量守恒定律的应用、反应物和生成物的判断、基本反应类型的判断等,难度不大.

练习册系列答案
相关题目
4.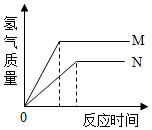 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )| A. | M、N两种金属中较活泼的是N | B. | 生成H2的速率N>M | ||
| C. | 相对原子质量较大的是N | D. | 生成H2的质量M<N |
5.下列鉴别物质的方法错误的是( )
| A. | 用水来鉴别碳酸钙粉末和碳酸钠粉末 | |
| B. | 用酚酞试液鉴别稀盐酸和氯化钠溶液 | |
| C. | 用燃烧的木条鉴别氧气和二氧化碳 | |
| D. | 用熟石灰区别化肥硝酸钾和硝酸铵 |
2.现将一包铜、铝的混合粉末加入到盛有MgCl2、FeCl2溶液的烧杯中,充分反应后溶液呈浅绿色,烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是( )
| A. | 溶液中溶质为MgCl2、FeCl2,固体为铝和铜 | |
| B. | 溶液中溶质为MgCl2、AlCl3、FeCl2,固体一定含有铝和铜 | |
| C. | 溶液中一定含FeCl2、CuCl2,固体一定含铜 | |
| D. | 溶液中一定含FeCl2,固体一定是铁和铜 |
9.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | CO2和SO2都能和NaOH溶液反应,CO也能和NaOH溶液反应 | |
| B. | CO和C都能和CuO反应生成Cu,有还原性,H2也能相CuO反应生成Cu,也有还原性 | |
| C. | 活泼金属和盐酸反应生成气体,和盐酸反应生成气体的物质不一定是活发金属 | |
| D. | 氢氧化钙和氢氧化钠都属于碱,都含有金属元素,所以碱都含有金属元素 |
19.根据如图提供的信息进行判断,下列说法中错误的是( )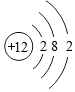

| A. | 该粒子原子核内有 12 个质子 | B. | 该粒子易形成阴离子 | ||
| C. | 该粒子属于金属元素 | D. | 该粒子不显电性 |
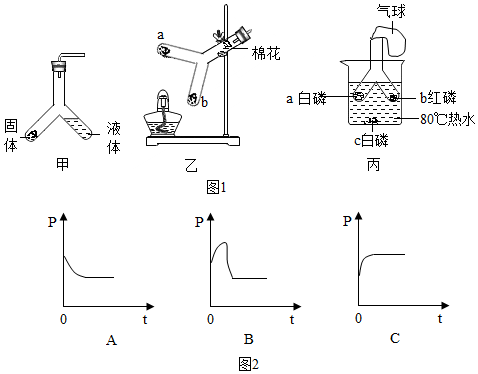
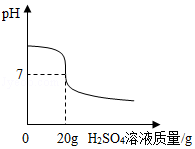 某小组欲用4.9%的稀H2SO4测一瓶标签破损的NaOH溶液的质量分数.
某小组欲用4.9%的稀H2SO4测一瓶标签破损的NaOH溶液的质量分数.