题目内容
欲测定某锌-铜合金中铜的质量分数,进行如下实验:取合金样品10g放入烧杯中,将60g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成气体质量/g | 0.08 | m | 0.04 |
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
【答案】(1)0.08
(2)解:合金共产生氢气的质量为0.08g+0.08g=0.04g=0.2g
设:该合金样品中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
X 0.2g
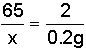
X=6.5g
样品中铜的质量10g-6.5g=3.5g,
铜的质量分数为3.5g/10g ×100%=35%
【解析】图表信息可知,第一次合金加入20g稀硫酸产生0.08g,第三次为0.04g,说明第三次合金已经完全反应,由此第二次时产生氢气的质量仍为0.08g,所以三次一共产生氢气的质量为0.08g+0.08g=0.04g=0.2g,利用此数据计算出合金中锌的质量从而作答。

练习册系列答案
相关题目