题目内容
1. 如图甲中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口与侧口不漏气).将图甲的装置在托盘天平上称量,质量为W1g.根据实验现象填写下列空白.
如图甲中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口与侧口不漏气).将图甲的装置在托盘天平上称量,质量为W1g.根据实验现象填写下列空白.(1)把气球b中的碳酸钙粉末小心倒入瓶中,立即产生许多气泡,气球逐渐胀大(如图乙),反应结束后,再将其称量,质量为W2g,若不考虑浮力,则W1与W2的关系是相等.
(2)将30g质量分数为20%的NaOH溶液,先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气),打开d,将溶液挤入瓶中,立即夹紧d,可看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样的方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失,使沉淀消失的反应的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,此事瓶内温度升高(填“不变”“降低”或“升高”).
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状,写出此时发生反应的化学方程式:2NaOH+CO2═Na2CO3+H2O;CO2+Ca(OH)2═CaCO3↓+H2O.
分析 (1)根据反应前后装置遵循质量守恒来回答;
(2)根据氢氧化钙的溶解性和酸碱中和反应的实质来回答;
(3)根据反应的实质和物质量的关系结合反应能量变化来分析;
(4)根据二氧化碳的性质能和碱反应来回答.
解答 解:(1)反应前后装置中的反应遵循质量守恒,故为:w2=w1故填:相等;
(2)溶液中存在溶解度较小的氢氧化钙,轻摇,沉淀又与盐酸反应而消失,发生的反应为:Ca(OH)2+2HCl=CaCl2+2H2O,故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;
(3)根据盐酸的量和氢氧化钠量的关系,可知氢氧化钠相对于酸过量,瓶内产生大量白色沉淀,不再溶解,反应是个放热过程,温度升高,故答案为:升高;
(4)产生的二氧化碳会和过量的碱反应,使气压减小,气球变小,方程式为:2NaOH+CO2═Na2CO3+H2O;CO2+Ca(OH)2═CaCO3↓+H2O.故填:2NaOH+CO2═Na2CO3+H2O;CO2+Ca(OH)2═CaCO3↓+H2O.
点评 此题考查碳酸钙、氢氧化钙、二氧化碳等物质的性质,要求学生具备实验的分析能力.

练习册系列答案
相关题目
12.向Mg(NO3)2和Cu(NO3)2的混合溶液中加入过量的Zn粉,充分反应后过滤、滤纸上的物质为( )
| A. | Cu | B. | Zn、Cu | C. | Mg、Cu | D. | Mg、Zn、Cu |
9.水是生活中常见的物质,下列有关水的说法正确的是( )
| A. | 水由氢原子和氧原子构成 | B. | 水由氢元素和氧元素构成 | ||
| C. | 水中氢、氧元素的个数比为2:1 | D. | 水中氢、氧元素的质量比比2:1 |
6.下列观点是某同学提出的,你认为不妥当的是( )
| A. | 常见的复合肥料有硝酸钾(KNO3)、磷酸二氢铵(NH4H2PO4)等 | |
| B. | 应将硫酸铵和熟石灰混施,在给作物提供氮元素的同时,又能降低土壤的酸性 | |
| C. | 若将农家肥和化肥综合施用,有助于提高化肥的增产效益 | |
| D. | 化肥使用不合理时,土壤结构会遭到破坏,还会因流失而污染江河湖泊 |
4.20℃时,1千克水中溶解50克A物质,恰好达到饱和,则A物质的溶解性等级为( )
| A. | 难溶 | B. | 微溶 | C. | 可溶 | D. | 易溶 |
5.一位农民种植的某块农田小麦产量总是比邻近地块的低.观察比较后,发现此农田的小麦长得矮小、容易倒伏、叶片上有斑点.农民将该块肥力均匀的农田分成面积相等的五小块,进行田间实验.除施肥不同外,其他田问管理措施相同.实验结果如表:
比较甲、乙、丁、戊可知,该农田可能缺少的元素是磷和钾,比较乙和丙可判断该农田缺少的元素是钾.
| 地 块 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 施肥情况(等质量) | 尿素 (含N) | 磷酸二氢钾 (含P、K) | 磷酸二氢铵 (含N、P) | 硫酸铵 (含N) | 不施肥 |
| 小麦收获量(千克) | 55.56 | 69.26 | 56.88 | 55.44 | 55.11 |
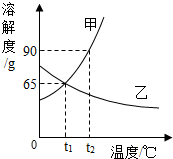 如图是甲、乙两种物质的溶解度曲线,请回答下列问题.
如图是甲、乙两种物质的溶解度曲线,请回答下列问题. 实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究
实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究