题目内容
13.神舟七号载人飞船成功返航,标志着我国已跨入航天领域国际领先行列.某研究性学习小组查阅资料得知,宇宙飞船中可用超氧化钾(KO2)作为氧气再生剂.超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气:4KO2+2CO2═2K2CO3+3O2,为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的CO2来与KO2反应制取O2,设计了如下实验装置: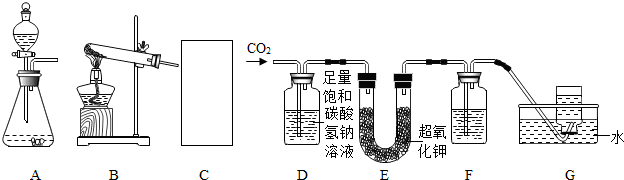
(1)C处应从A、B两种装置中选择A作CO2发生装置.检验G中集气瓶内收集的气体是否为氧气,可以在取出集气瓶后,用带火星的木条检验.
(2)已知CO2不溶于饱和碳酸氢钠溶液,D装置的作用是除去CO2中混有的HCl.
(3)为了除去O2中可能混有的CO2,F中可盛放过量NaOH溶液.
(4)有同学提出,上述实验能生成氧气可能与CO2中混有的水蒸气有关.若要检验干燥的CO2能否与超氧化钾反应生成氧气,你对上述实验装置的改进方法是在D和E装置之间增加气体干燥装置.
分析 根据题意,目的是验证制取出的二氧化碳与超氧化钾反应生成氧气并验证氧气.为了得到纯净的二氧化碳和氧气,要对反应生成的气体进行净化.根据气体的性质选择适当的净化剂.利用浓硫酸的吸水性除去CO2中混有的水蒸气即可.
解答 解:(1)制取二氧化碳用固体和液体反应,并且不需要加热,所以应选择A装置;检验氧气使用的是带火星的木条;
(2)为了防止二氧化碳中的氯化氢气体对后面实验的干扰,故用饱和碳酸氢钠溶液把它除去;
(3)除去O2中可能混有的CO2的方法是通过氢氧化钠溶液,二氧化碳能和氢氧化钠溶液反应,氧气不能;
(4)浓硫酸有吸水性,可以除去二氧化碳中的水分而不会除去二氧化碳.
故答案为:
(1)A;带火星的木条;
(2)除去CO2中混有的HCl;
(3)NaOH;
(4)在D和E装置之间增加气体干燥装置.
点评 除去一种气体中的其他杂质,要根据气体的性质进行选择,既要把杂质除去,又不能影响被除杂质的气体.

练习册系列答案
相关题目
6.下列有关说法正确的是( )
| A. | 在金属表面涂油或刷漆可以隔绝空气和水蒸气,防止金属锈蚀 | |
| B. | 催化剂在化学反应前后其化学性质发生了变化 | |
| C. | 不饱和溶液变为饱和溶液,溶质质量分数一定变大 | |
| D. | 烧碱、浓硫酸都可用来干燥氨气 |
4.同学们整理实验室时,发现一瓶白色固体粉末状药品.实验老师告诉大家药品可能是碳酸钠、碳酸钙、氯化钠、氢氧化钠、硫酸钡中的一种或几种.同学们对此很好奇,于是他们对这瓶白色粉末的成分做了如下探究.
【实验I】小伟取一定量白色粉末于烧杯中,加足量水搅拌,过滤,得到固体和无色滤液.
【实验II】小伟取少量实验I得到的无色滤液于试管中,滴加无色酚酞后,观察到变成红色.于是小伟马上就得出结论,该瓶白色粉末一定有氢氧化钠.但是小旭却认为小伟的结论不一定正确,你认为小旭的理由是(1)碳酸钠的溶液也为碱性.于是小旭另取少量滤液于试管中,加入过量氯化钡溶液,有白色沉淀产生;取上层清液,加入少量氯化铁溶液产生红褐色沉淀.
根据现象,你认为滤液中的溶质有(2)NaOH、Na2CO3,(填化学式,下同)请用相关化学方程式解释这些现象(3)BaCl2+Na2CO3=BaCO3↓+2NaCl;
3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
【实验III】小伟和小旭认为有必要再对实验I中滤渣的成分进行探究,过程如下:
【交流】实验结束后,同学们一致认为通过实验Ⅱ能确定原试剂瓶中还含有(4)NaOH、Na2CO3,但小伟和小旭同学认为,通过上述实验还是不能证明原瓶中是否含有(5NaCl.
【实验I】小伟取一定量白色粉末于烧杯中,加足量水搅拌,过滤,得到固体和无色滤液.
【实验II】小伟取少量实验I得到的无色滤液于试管中,滴加无色酚酞后,观察到变成红色.于是小伟马上就得出结论,该瓶白色粉末一定有氢氧化钠.但是小旭却认为小伟的结论不一定正确,你认为小旭的理由是(1)碳酸钠的溶液也为碱性.于是小旭另取少量滤液于试管中,加入过量氯化钡溶液,有白色沉淀产生;取上层清液,加入少量氯化铁溶液产生红褐色沉淀.
根据现象,你认为滤液中的溶质有(2)NaOH、Na2CO3,(填化学式,下同)请用相关化学方程式解释这些现象(3)BaCl2+Na2CO3=BaCO3↓+2NaCl;
3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
【实验III】小伟和小旭认为有必要再对实验I中滤渣的成分进行探究,过程如下:
| 步骤 | 实验现象 |
| (1)取少量液于试管,向其滴加足量稀盐酸溶液,振荡 | 有气体冒出,试管底还残留少量固体 |
| (2)过滤,取少量滤液于试管中,加入硝酸银和稀硝酸溶液 | 有白色沉淀生成 |
1. 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A.产生的气体可能是H2 B.产生的气体可能是CO2
C.CuSO4溶液中可能含有少量的某种酸 D.CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下研究.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3.作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl.作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表示).
【实验设计】
(4)某同学取100g含有H2SO4的酸性废水,然后滴加烧碱溶液中和,至溶液pH=7时,共消耗质量分数为20%的烧碱溶液20g.求这种废水中含H2SO4的质量分数.
 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A.产生的气体可能是H2 B.产生的气体可能是CO2
C.CuSO4溶液中可能含有少量的某种酸 D.CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下研究.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3.作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl.作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表示).
【实验设计】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁试 | 管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还还有的杂质是氯化钠 |
8.铜是人类普遍使用最早的金属.我们的祖先一开始使用的是纯铜,即红铜.红铜之后,发展到使用铜锡合金的青铜.青铜熔点比红铜低,硬度大,而且又比较耐腐蚀,而我国的锡储量占世界第一位.古代记载的炼锡方法基本上就是现代用的碳还原法,该反应的化学方程式为:SnO2+2C$\frac{\underline{\;高温\;}}{\;}$Sn+2CO↑.该反应类型属于( )
| A. | 复分解反应 | B. | 置换反应 | C. | 分解反应 | D. | 化合反应 |
18.下列有关说法或实验方法不合理的是( )
| A. | “缺铁性贫血”里所说的铁不是单质铁 | |
| B. | 家用铝锅不可以用来盛放酸性食物 | |
| C. | 水可用来鉴别硝酸钾固体和氢氧化钠固体 | |
| D. | 铁丝和铜丝分别插入氢氧化钠溶液中,都无变化,说明铁和铜一样不活泼 |
2.下列说法正确的是( )
| A. | 淀粉遇加碘食盐溶液会变蓝 | |
| B. | 瘦肉中主要含蛋白质,不含无机盐之类的营养素 | |
| C. | 某气体能使灼热的氧化铜还原成铜,这种气体一定是一氧化碳 | |
| D. | 鉴别氢氧化钠固体和硝酸铵固体,可加适量水溶解,用手触摸试管外壁温度的变化 |
3.我区某校九年级(1)班的同学们学习“中和反应”后,在实验室里他们将一定量的稀硫酸滴到氢氧化钠溶液中,如图1所示,其反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
同学们发现该实验观察不到明显的现象,于是进行了一系列探究活动: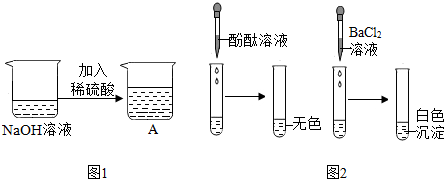
【提出问题】如何验证该反应已经发生?
【实验探究】甲组同学分别取图1所示A烧杯中的溶液进行了两个探究活动(实验1和实验2),现象如图2所示.
【反思评价】甲组同学认为图2中“实验1”能验证反应已经发生了,他们的理由是加入酚酞试液不变色.
【再次提问】图1所示A烧杯中溶液的溶质成分有哪些?
【再次探究】乙组同学进行如下实验,已知他们所加入试剂的类别不同于“实验1”和“实验2”所加试剂的类别.请填空:
【解释与结论】
将“实验2”中烧杯静置一段时间后,上层清液中一定有的溶质是NaCl.(填化学式)
同学们发现该实验观察不到明显的现象,于是进行了一系列探究活动:

【提出问题】如何验证该反应已经发生?
【实验探究】甲组同学分别取图1所示A烧杯中的溶液进行了两个探究活动(实验1和实验2),现象如图2所示.
【反思评价】甲组同学认为图2中“实验1”能验证反应已经发生了,他们的理由是加入酚酞试液不变色.
【再次提问】图1所示A烧杯中溶液的溶质成分有哪些?
【再次探究】乙组同学进行如下实验,已知他们所加入试剂的类别不同于“实验1”和“实验2”所加试剂的类别.请填空:
| 实验操作 | 实验现象 | 结论 |
| 取A烧杯中的少量溶液于试管中,加入铁粉. | 观察到有气泡产生 | A烧杯中溶液的溶质是Na2SO4和H2SO4. |
将“实验2”中烧杯静置一段时间后,上层清液中一定有的溶质是NaCl.(填化学式)
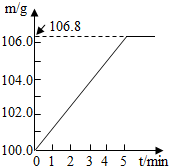 某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸完全吸收.测得吸收氨气后溶液总质量m与反应时间t的变化如图所示.所涉及的反应为:
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸完全吸收.测得吸收氨气后溶液总质量m与反应时间t的变化如图所示.所涉及的反应为: