题目内容
9.“洁厕灵”的有效成分为盐酸,可以清除污垢,除去异味.(1)“洁厕灵”能轻松除去铁制品表面的铁锈,但不能长时间浸泡,用化学方程式表示原因Fe2O3+6HCl=2FeCl3+3H2O、Fe+2HCl═FeCl2+H2↑.
(2)“漂白精”的有效成分为次氯酸钠(NaClO),可以快速漂除衣物污渍,若与“洁厕灵”混用,易产生一种有毒气体,反应的化学方程式为NaClO+2HCl═NaCl+Cl2↑+X,则X的化学式为H2O.
分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:(1)“洁厕灵”的有效成分为盐酸,铁锈的主要成分是氧化铁(Fe2O3),将铁制品放入“洁厕灵”中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;当铁锈完全反应后,铁与稀盐酸发生反应,生成氯化亚铁与氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
(2)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式NaClO+2HCl═NaCl+Cl2↑+X,反应前钠、氯、氧、氢原子个数分别为1、3、1、2,反应后的生成物中钠、氯、氧、氢原子个数分别为1、3、0、0,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为H2O.
故答案为:(1)Fe2O3+6HCl=2FeCl3+3H2O;Fe+2HCl=FeCl2+H2↑;(2)H2O.
点评 本题难度不大,掌握化学方程式的书写方法、化学反应前后原子守恒是正确解答本题的关键.

练习册系列答案
相关题目
20.工业中制备KClO3的流程如下:
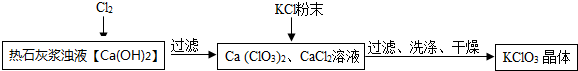
已知常温下几种物质的溶解度分别为:Ca(ClO3)2 是209.0g;KClO3 是7.4g;CaCl2 是74.5g;则下列说法中错误的是( )

已知常温下几种物质的溶解度分别为:Ca(ClO3)2 是209.0g;KClO3 是7.4g;CaCl2 是74.5g;则下列说法中错误的是( )
| A. | 上述流程中氯元素化合价既有升高,又有降低 | |
| B. | 过滤操作中需要的玻璃仪器有:漏斗、烧杯、玻璃棒、酒精灯 | |
| C. | 洗涤KClO3晶体时用饱和KCl溶液比用饱和KClO3溶液效果更好 | |
| D. | 上述流程中生成KClO3的反应是:2KCl+Ca(ClO3)2=2KClO3↓+CaCl2 |
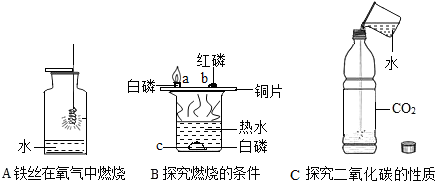
17. 用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )
用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )
 用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )
用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )| A. | 事先在集气瓶内加少量水 | |
| B. | 实验前,检查装置的气密性 | |
| C. | 红磷熄灭后,立即打开弹簧夹 | |
| D. | 该实验可将红磷换成硫粉,烧杯中的水换成浓氢氧化钠溶液 |
4.下列化学符号中,数字“2”表示的意义不正确的是( )
| A. | 2Na:两个钠元素 | |
| B. | 2OH-:两个氢氧根离子 | |
| C. | $\stackrel{+2}{Mg}$:镁元素的化合价为+2价 | |
| D. | NO2:一个二氧化氮分子含有两个氧原子 |
14.下列符号书写正确且与名称相一致的是( )
| A. | 镁 Ng | B. | 麟 P | C. | 铜 Co | D. | 氟 F |
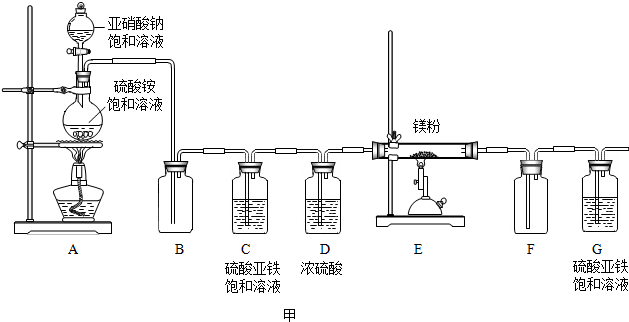
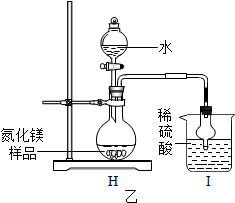
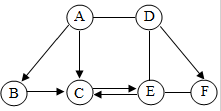 如图所示:A、B、C、D、E、F为初中化学常见的六种化合物,A、B、C均为氧化物,其中“A→B”这一反应常用于工业炼铁;D、E、F均由三种元素组成,且物质类别各不相同,E、F可用来配制波尔多液.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
如图所示:A、B、C、D、E、F为初中化学常见的六种化合物,A、B、C均为氧化物,其中“A→B”这一反应常用于工业炼铁;D、E、F均由三种元素组成,且物质类别各不相同,E、F可用来配制波尔多液.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题: