题目内容
镁条在空气中易被氧化.有一根在空气中放置一段时间的镁条样品,其质量为2.8g,将该样品放入107.8g稀硫酸中,两者恰好完全反应,反应过程中测得数据如下:
请计算 (写出计算过程):
(1)反应前后减少的质量是 g,原因是
(2)2.8g样品中含氧化镁的质量是多少?
(3)稀硫酸中溶质的质量分数是多少?
| 数据记录时间 | t1 | t2 | t3 | t4 |
| 剩余物质质量/g | 110.52 | 110.46 | 110.40 | 110.40 |
(1)反应前后减少的质量是
(2)2.8g样品中含氧化镁的质量是多少?
(3)稀硫酸中溶质的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据题意,一根在空气中放置一段时间的镁条样品,其质量为2.8g,将该样品放入107.8g稀硫酸中,两者恰好完全反应,由反应过程中测得数据,最终剩余物质的质量为110.40g,由质量守恒定律,产生氢气的质量为2.8g+107.8g-110.40g=0.2g;据此由镁与稀硫酸、氧化镁与稀硫酸反应的化学方程式,进行分析解答即可.
解答:解:(1)反应前后减少的质量是2.8g+107.8g-110.40g=0.2g,原因是产生的氢气逸出.
(2)设2.8g样品中含镁的质量为x,与镁反应消耗的硫酸的质量为y
Mg+H2SO4═MgSO4+H2↑
24 98 2
x y 0.2g
=
x=2.4g
2.8g样品中含氧化镁的质量是2.8g-2.4g=0.4g.
(3)
=
y=9.8g
设与氧化镁反应消耗的硫酸的质量为z
MgO+H2SO4═MgSO4+H2O
40 98
0.4g z
=
z=0.98g
稀硫酸中溶质的质量分数是
×100%=10%.
答:(1)0.2;产生的氢气逸出;(2)2.8g样品中含氧化镁的质量是0.4g;(3)稀硫酸中溶质的质量分数是10%.
(2)设2.8g样品中含镁的质量为x,与镁反应消耗的硫酸的质量为y
Mg+H2SO4═MgSO4+H2↑
24 98 2
x y 0.2g
| 24 |
| 2 |
| x |
| 0.2g |
2.8g样品中含氧化镁的质量是2.8g-2.4g=0.4g.
(3)
| 98 |
| 2 |
| y |
| 0.2g |
设与氧化镁反应消耗的硫酸的质量为z
MgO+H2SO4═MgSO4+H2O
40 98
0.4g z
| 40 |
| 98 |
| 0.4g |
| z |
稀硫酸中溶质的质量分数是
| 9.8g+0.98g |
| 107.8g |
答:(1)0.2;产生的氢气逸出;(2)2.8g样品中含氧化镁的质量是0.4g;(3)稀硫酸中溶质的质量分数是10%.
点评:本题难度不大,主要考查学生根据图表数据、化学方程式的计算进行解决问题的能力,由质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
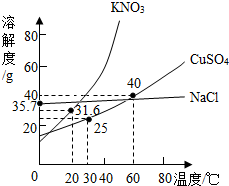 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A、40℃时将35gNaCl溶 于100g水中,降温至0℃时,可析出NaCl晶体 |
| B、20℃时KNO3饱和溶液的质量分数是31.6% |
| C、60℃时,200g水中溶解80gCuSO4达饱和,当降至30℃时,可析出30gCuSO4晶体 |
| D、30℃时,将35g KNO3和35gNaCl同时溶于100g水中,蒸发时先析出的是NaCl |

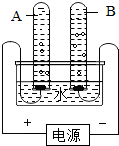 水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题:
水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题: