题目内容
日常生活中离不开金属.

(1)铝、铁、铜是我们生产生活中使用比较广泛的金属,如图1所示用品中,其用途主要利用金属导热性的是 (填字母序号).
(2)铝化学性质活波,但铝制品不易锈蚀,其原因是 .防止自行车链条生锈常用的方法是 .
某化学兴趣小组利用图2装置进行实验探究,请按要求填空.
(3)写出CO还原Fe2O3的化学方程式 ;
(4)对该装置的主要不足之处,你的改进方法是在右图A处 ;
(5)用酒精喷灯加热前,要先通入CO,目的是 .

(1)铝、铁、铜是我们生产生活中使用比较广泛的金属,如图1所示用品中,其用途主要利用金属导热性的是
(2)铝化学性质活波,但铝制品不易锈蚀,其原因是
某化学兴趣小组利用图2装置进行实验探究,请按要求填空.
(3)写出CO还原Fe2O3的化学方程式
(4)对该装置的主要不足之处,你的改进方法是在右图A处
(5)用酒精喷灯加热前,要先通入CO,目的是
考点:金属的物理性质及用途,金属的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据物质的性质决定物质的用途考虑;
(2)根据铝的化学性质进行分析;铝表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.铁的锈蚀实际是铁与空气中的水和氧气共同作用的结果;要防止铁生锈就要从隔绝空气的角度分析.
(3)只有熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则和化学方程式的书写方法,就能写出正确的化学方程式.
(4)尾气中含有一氧化碳;
(5)根据可燃性气体不纯加热可能会发生爆炸进行分析解答.
(2)根据铝的化学性质进行分析;铝表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.铁的锈蚀实际是铁与空气中的水和氧气共同作用的结果;要防止铁生锈就要从隔绝空气的角度分析.
(3)只有熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则和化学方程式的书写方法,就能写出正确的化学方程式.
(4)尾气中含有一氧化碳;
(5)根据可燃性气体不纯加热可能会发生爆炸进行分析解答.
解答:解:(1)不锈钢锅是利用了金属的导热性;铜导线是利用了铜的导电性;铝制铝箔是利用铝的延展性.故填:A;
(2)通常情况下铝制品很耐腐蚀,这是因为铝在常温下与空气中的氧气发生化学反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;洗涤铝制品时注意注意不能刷掉氧化铝薄膜.铁的锈蚀实际是铁与空气中的水和氧气共同作用的结果;要防止铁生锈就要使铁隔绝空气,如在铁表面涂一层油漆,或在铁表面镀一层耐腐蚀的金属,或用油擦拭铁表面等.
故填:铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;涂抹矿物油;
(3)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳.该反应的化学方程式为:3CO+Fe2O3
3CO2+2Fe.故填:3CO+Fe2O3
3CO2+2Fe;
(4)由于一氧化碳是对空气有污染的气体.所以,需要将尾气点燃处理,故填:将尾气点燃或收集;
(5)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此应先通CO排尽玻璃管中的空气,然后再点燃加热氧化铁的酒精喷灯.
答案为:赶尽玻璃管内的空气,防止加热爆炸.
(2)通常情况下铝制品很耐腐蚀,这是因为铝在常温下与空气中的氧气发生化学反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;洗涤铝制品时注意注意不能刷掉氧化铝薄膜.铁的锈蚀实际是铁与空气中的水和氧气共同作用的结果;要防止铁生锈就要使铁隔绝空气,如在铁表面涂一层油漆,或在铁表面镀一层耐腐蚀的金属,或用油擦拭铁表面等.
故填:铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;涂抹矿物油;
(3)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳.该反应的化学方程式为:3CO+Fe2O3
| ||
| ||
(4)由于一氧化碳是对空气有污染的气体.所以,需要将尾气点燃处理,故填:将尾气点燃或收集;
(5)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此应先通CO排尽玻璃管中的空气,然后再点燃加热氧化铁的酒精喷灯.
答案为:赶尽玻璃管内的空气,防止加热爆炸.
点评:本题以一氧化碳还原氧化铁为切入点,考查实验中的注意事项、实验现象、反应原理以及环保的问题,考查知识点全面,属基础知识考查题.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列各组物质是按单质、氧化物、混合物的顺序排列的是( )
| A、臭氧、干冰、冰水混合物 |
| B、氮气、氯酸钾、食盐水 |
| C、氧气、水、空气 |
| D、白酒、生石灰、碘酒 |
观察和实验是学习科学的重要方式,下列试验中观察到的颜色正确的是( )
| A、铁锈放在稀硫酸中溶液变黄色 |
| B、酚酞试液滴入硫酸溶液中变红色 |
| C、铜放入稀硫酸中溶液变蓝色 |
| D、硫酸铜溶液中滴加氢氧化钠溶液出现红褐色絮状沉淀 |
下列关于氧气的物理性质说法中,正确的是( )
| A、液态氧是一种淡蓝色液体 |
| B、氧气难溶于水 |
| C、氧气在通常状况下是一种稍显蓝色的气体 |
| D、氧气的密度略小于空气 |
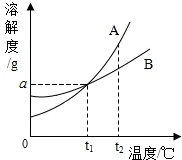 如图是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
如图是A、B两种固体物质的溶解度曲线,下列说法正确的是( )| A、A物质的溶解度大于B物质 |
| B、t1℃时,A、B两种溶液中溶质的质量分数相同 |
| C、t1℃时,两种物质的溶解度都为ag |
| D、t2℃时,A的饱和溶液中溶质的质量分数小于B的饱和溶液中溶质的质量分数 |
下列说法正确的是( )
| A、铜粉在空气中加热后固体质量会增加,因此这个反应不遵守质量守恒定律 |
| B、钢铁是刚和铁熔合在一起制得的具有金属特性的合金 |
| C、铁钉在潮湿的空气中容易生锈 |
| D、处理金属废弃物的方法是填埋法 |