题目内容
6.人类的日常生产、生活都离不开水.化学课上同学们分组研究水的净化及组成(装置如图).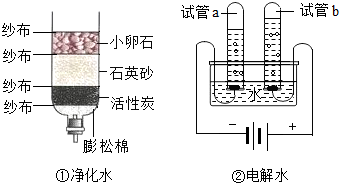
(1)其中一组同学用自制简易净水器(图①所示)净化池塘水,其中小卵石、石英砂、纱布的作用是过滤.
(2)自然界中的水有硬水和软水.含有较多可溶性钙、镁化合物的水叫做硬水,净化后得到的净水是硬水还是软水,常用肥皂水来区分.
(3)实验②中通电一段时间后,试管a中产生的气体是H2(写化学式),试管b中产生的气体能使带火星的木条复燃,该实验说明水是由氢元素和氧元素组成的,该反应的方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 (1)根据过滤可以除去不溶于水的物质解答;
(2)根据可以用肥皂水检验硬水和软水解答;
(3)根据电解水的实验、水的组成进行分析解答.
解答 解:
(1)小卵石、石英砂的作用是过滤.故填:过滤.
(2)自然界中的水有硬水和软水.含有较多可溶性钙、镁化合物的水叫做硬水,净化后得到的净水是硬水还是软水,常用肥皂水来区分,泡沫多的是软水,泡沫少的是硬水;
(3)电解水时,与电源正极相连的试管内产生的气体体积少,能使带火星的木条复燃,是氧气;与电源负极相连的试管内的气体体积多,能燃烧,是氢气;则与两个电极相连的a、b两支玻璃管中产生的气体分别是氢气、氧气,且两者的体积之比大约是2:1.
电解水生成氢气和氧气,氢气是由氢元素组成的,氧气是由氧元素组成的,该实验证明了水是由氢元素和氧元素组成的.反应的方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
答案:
(1)过滤;
(2)可溶性; 肥皂水;
(3)H2;复燃; 氢元素和氧元素; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 解答本题要充分理解净化水的方法方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 为节约药品,实验剩余的药品应放回原瓶 | |
| B. | 为防止液体滴出,取液后的滴管应平放或倒置 | |
| C. | 为防止事故发生,实验室中鉴别一种试剂是否是食盐,不能尝味道 | |
| D. | 为闻到药品的气味,应将鼻孔凑到容器口去闻 |
14.硬水对生活的危害很大.生活中要使硬水软化,经常采用的办法是( )
| A. | 蒸馏 | B. | 煮沸 | C. | 过滤 | D. | 消毒 |
1.对“质量守恒定律”的理解,正确是( )
| A. | 10g冰受热熔化成10g水 | |
| B. | 参加反应的氢气和氧气的体积,一定等于生成水的体积 | |
| C. | 反应前后原子种类、原子数目、分子的数目均不变 | |
| D. | 任何化学反应中参加反应的物质的总质量等于生成物质的总质量 |
11.一包不纯的Na2CO3固体,杂质可能是CuSO4、KNO3、CaCl2、NaHCO3中的一种或几种.现取该样品溶于水得到无色澄清溶液;另取样品10.6g,加入100g稀硫酸恰好完全反应,产生气体4.6g,则下列判断正确的是( )
| A. | 样品中一定没有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 样品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 样品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶质的质量分数大于9.8% |
16.在下空格内填写正确的名称、化学式、类别(指单质、酸、碱、盐、氧化物、有机物等).
| 序号 | (1) | (2) | (3) | (4) | (5) | (6) |
| 名称 | 氧化亚铁 | 铅 | 硝酸 | 纯碱 | 氨水 | 葡萄 |
| 化学式 | FeO | Pb | HNO3 | Na2CO3 | NH3•H2O | C6H12O6 |
| 类别 | 氧化物 | 单质 | 酸 | 盐 | 碱 | 有机物 |