题目内容
14.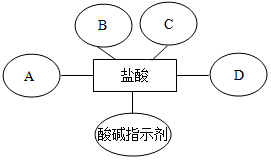 构建知识网络是一种重要的学习方法,如图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,A、B、C、D属于不同类别的物质,完善这个知识网络:
构建知识网络是一种重要的学习方法,如图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,A、B、C、D属于不同类别的物质,完善这个知识网络:(1)写出A、B、C、D的化学式:ANaOH;BFe2O3;CNa2CO3;DZn.
(2)根据自己得出的知识网络,写出一个化学方程式NaOH+HCl=NaCl+H2O.
分析 由酸的通性可知酸能跟活泼金属、金属氧化物、盐、碱反应.则可知A、B、C、D是金属氧化物、碱、盐、活泼金属,据此解答即可;
解答 解:(1)则依据酸的通性我们可假设A为一种碱设A为氢氧化钠,则B为金属氧化物,B可为氧化铁等,C为盐,C可为碳酸钠,D为金属,D可为锌等能够完成该网络;
(2)氢氧化钠与盐酸反应生成氯化钠和水,方程式为NaOH+HCl=NaCl+H2O.
故答案为:(1)NaOH;Fe2O3;Na2CO3;Zn(其他合理答案均可);(2)NaOH+HCl=NaCl+H2O(其他合理答案均可)
点评 解答此类题要求同学们在平时的学习过程中,要学会知识的综合应用,才能准确的写出符合题意的答案.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
4.学习化学知识后,观察物质世界就要从化学视角看.下列对天然气的主要成分--甲烷(CH4)的看法正确的是( )
| A. | 从组成上看:甲烷由碳、氢两种元素组成 | |
| B. | 从构成上看:甲烷由1 个碳原子、4 个氢原子构成 | |
| C. | 碳元素和氢元素的质量比为1:3 | |
| D. | 天然气中氢元素的质量分数=$\frac{1}{17}$×100%=5.9% |
2.我国“西气东输”工程输送的天然气主要成分是甲烷(CH4),对该化学式的意义讨论,错误的是( )
| A. | 表示甲烷这种物质 | |
| B. | 表示甲烷由一个碳原子和4个氧原子构成 | |
| C. | 表示一个甲烷分子 | |
| D. | 表示甲烷由碳元素和氢元素组成 |
9.在盛有下列固体的试管内,加入足量的稀盐酸,能得到无色溶液的是( )
| A. | Fe | B. | Fe2O3 | C. | Cu(OH)2 | D. | Na2CO3 |
19.小刚从教材上了解到,过氧化氢溶液受热容易分解生成水和氧气,他将10mL5%的过氧化氢溶液放入试管中,放在酒精灯火焰上加热,然后用带火星的木条伸入试管内,木条不复燃,针对这一发现,你认为以下做法中不可取的是( )
| A. | 反复多次实验查找原因 | |
| B. | 用高锰酸钾代替过氧化氢溶液进行实验 | |
| C. | 大胆提出假设:由于反应条件是加热,有大量水蒸气同时逸出 | |
| D. | 查找过氧化氢溶液是否变质 |
6.我国继“加碘食盐”后,又启动了“加铁酱油”工程.这里的“碘”、“铁”是指( )
| A. | 原子 | B. | 离子 | C. | 元素 | D. | 分子 |
4.硝酸铵是一种重要的化肥,微溶于酒精易溶于水,下表是它在水中的溶解度.
下列有关硝酸铵的说法错误的是( )
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度(g) | 118.3 | 141 | 192 | 241.8 | 286 | 344 | 421 | 580 | 871 |
| A. | 20℃时硝酸铵在水中的溶解度大于在酒精中的溶解度 | |
| B. | 硝酸铵在水中的溶解度随温度升高而增大 | |
| C. | 50℃时硝酸铵溶液降温后溶质质量分数减小 | |
| D. | 应避免硝酸铵肥料在碱性环境中施用 |
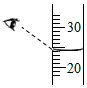 量取95mL的水,最好选用100mL的量筒.某同学.用30mL的量筒量取25mL的水,请你仔细观察该图,判断量筒内液体的体积实际是<(填>、﹦、<)25mL.
量取95mL的水,最好选用100mL的量筒.某同学.用30mL的量筒量取25mL的水,请你仔细观察该图,判断量筒内液体的体积实际是<(填>、﹦、<)25mL.