题目内容
课外活动小组的同学在测定由氯化钠和碳酸钠形成的固体混合物组成时,进行了以下实验:取80g固体混合物配成溶液,平均分成四份,然后分别加入一定质量分数的氯化钙溶液,实验数据见下表.(混合物中其它成分不与氯化钙反应且易溶于水)
请根据表中数据回答:(相对原子质量:Ca:40 Cl:35.5 Na:23 C:12 O:16)
(1)m= g.
(2)40g原固体混合物配成的溶液和足量氯化钙溶液反应,最多生成沉淀质量为 g.
(3)原固体混合物中,碳酸钠的质量分数是多少?(写出计算过程)
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入氯化钙溶液 | 20g | 40g | 60g | 80g |
| 生成沉淀质量 | 4g | m | 10g | 10g |
(1)m=
(2)40g原固体混合物配成的溶液和足量氯化钙溶液反应,最多生成沉淀质量为
(3)原固体混合物中,碳酸钠的质量分数是多少?(写出计算过程)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据实验数据,加入20gCaCl2溶液完全反应可生成沉淀质量为4g,加入40gCaCl2溶液时仍有沉淀生成,可判断表中m的值;
(2)生成最多的沉淀的质量,应是完全反应后生成的沉淀质量,所以最多生成沉淀质量可由分析图表得到;
(3)加入氯化钙溶液至完全反应时,生成沉淀质量为10g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中Na2CO3的质量分数.
(2)生成最多的沉淀的质量,应是完全反应后生成的沉淀质量,所以最多生成沉淀质量可由分析图表得到;
(3)加入氯化钙溶液至完全反应时,生成沉淀质量为10g,根据碳酸钠与氯化钙反应的化学方程式,可由生成沉淀碳酸钙的质量计算中原固体混合物中Na2CO3的质量,即可求得原固体混合物中Na2CO3的质量分数.
解答:解:(1)在反应过程中,参加反应的物质与生成物的质量成正比,由图表可知:每20gCaCl2溶液可生4g沉淀,故m=8g;
故答案为:8;
(2)据图表可知,加入CaCl2溶液的质量到60g和80g时的沉淀质量一样多,说明加到60g 时已完全反应,故最多生成沉淀质量为10g;
故答案为:10;
(3)设20g原固体混合物中Na2CO3质量为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
x 10g
=
解得:x=10.6g
固体混合物中Na2CO3的质量分数是:
×100%=53%
答:原混合物中碳酸钠的质量分数是53%.
故答案为:8;
(2)据图表可知,加入CaCl2溶液的质量到60g和80g时的沉淀质量一样多,说明加到60g 时已完全反应,故最多生成沉淀质量为10g;
故答案为:10;
(3)设20g原固体混合物中Na2CO3质量为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
x 10g
| 106 |
| 100 |
| x |
| 10g |
解得:x=10.6g
固体混合物中Na2CO3的质量分数是:
| 10.6g |
| 20g |
答:原混合物中碳酸钠的质量分数是53%.
点评:本题主要考查学生根据化学方程式的计算及分析数据解答问题的能力,要据题意细心分析解答.

练习册系列答案
相关题目
下列物质在氧气中燃烧的实验现象描述正确的是( )
| A、镁条在氧气中燃烧时,有黑色固体生成 |
| B、蜡烛在氧气中燃烧时,有水和二氧化碳产生 |
| C、铁丝在氧气中燃烧时,火星四射,有黑色熔融物生成 |
| D、硫粉在在空气中燃烧时,有蓝紫色火焰产生,生成刺激性气味的气体 |
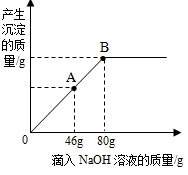 向盛有102g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶掖,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示,请根据题意回答下列问题:
向盛有102g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶掖,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示,请根据题意回答下列问题: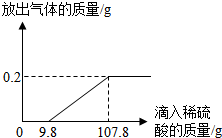 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: