题目内容
| 元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
(2)氢氧化钠的化学式是
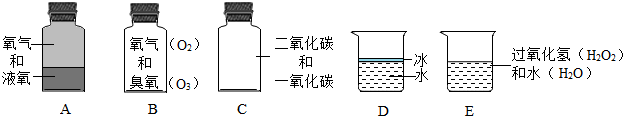
(3)下列分别盛有不同物质的容器中,所盛物质属于单质的是
考点:元素的符号及其意义,从组成上识别氧化物,纯净物和混合物的判别,单质和化合物的判别,化学式的书写及意义,有关元素化合价的计算
专题:化学用语和质量守恒定律,物质的分类
分析:(1)根据地壳里各元素的含量由多到少的顺序排列依次是氧,硅,铝,铁,水中含有的元素是氢元素、氧元素进行分析;
(2)根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简进行分析;
根据在化合物中正负化合价代数和为零进行分析;
(3)根据纯净物只含有一种物质;当确认它是纯净物时,再看它其中含有几种元素,含有一种的是单质;含有多种的是化合物;含有多种物质的为混合物进行分析.
(2)根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简进行分析;
根据在化合物中正负化合价代数和为零进行分析;
(3)根据纯净物只含有一种物质;当确认它是纯净物时,再看它其中含有几种元素,含有一种的是单质;含有多种的是化合物;含有多种物质的为混合物进行分析.
解答:解:(1)地壳里各元素的含量由多到少的顺序排列依次是氧,硅,铝,铁,所以在地壳内含量最多的非金属元素符号是:O,水中含有的+1价的元素是氢元素,所以元素符号为:H;
(2)根据化合物化学式的书写步骤,钠元素显示+1价,氢氧根离子显示-1价,所以氢氧化钠的化学式是:NaOH,根据在化合物中正负化合价代数和为零,钠元素的化合价为+1,氧元素的化合价为-2,可得Na2SO3中S元素的化合价为:(+1)×2+x+(-2)×3=0,
所以x=+4;
(3)通过分析各容器内的物质可知,A是单质,B是混合物,C是混合物,D是化合物、氧化物,E是混合物.
故答案为:(1)O,H;
(2)NaOH,+4;
(3)A,D,BCE,D.
(2)根据化合物化学式的书写步骤,钠元素显示+1价,氢氧根离子显示-1价,所以氢氧化钠的化学式是:NaOH,根据在化合物中正负化合价代数和为零,钠元素的化合价为+1,氧元素的化合价为-2,可得Na2SO3中S元素的化合价为:(+1)×2+x+(-2)×3=0,
所以x=+4;
(3)通过分析各容器内的物质可知,A是单质,B是混合物,C是混合物,D是化合物、氧化物,E是混合物.
故答案为:(1)O,H;
(2)NaOH,+4;
(3)A,D,BCE,D.
点评:本题主要考查学生对化学用语的书写、所学化学知识的理解及在解题中应用的能力.

练习册系列答案
相关题目
下列有关分子和原子的说法中,正确的是( )
| A、分子是保持物质性质的最小粒子 |
| B、原子是化学变化中的最小粒子 |
| C、分子一定比原子大 |
| D、分子可以再分而原子不能再分 |
小雨的妈妈买了一条黄金项链,小雨想通过实验探究这条黄金项链是否为锌铜合金制成的仿制品,她不能选用的试剂是( )
| A、AlCl3溶液 |
| B、Cu(NO3)2溶液 |
| C、H2SO4溶液 |
| D、AgNO3溶液 |
下列物质的用途中,主要利用其物理性质的是( )
| A、氧气用于气焊 |
| B、干冰用于人工降雨 |
| C、氮气用于保护气 |
| D、一氧化碳用于炼铁 |
下列各组元素,其中大写字母一样的是( )
| A、镁银汞 | B、锰铜锌 |
| C、氮氖钠 | D、碳钙铝 |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如表
关于此反应,下列认识不正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | 待测 | 16 | 6 | 35 |
| A、该变化的基本反应类型是化合反应 |
| B、参加反应的甲、丙的质量比为1:9 |
| C、反应后生成的乙、丁的质量比一定为3:5 |
| D、甲反应后的质量为0 |
镁在空气中燃烧生成氧化镁.其固体质量变化可用如图表示,则(80-48)g 表示的质量为( )
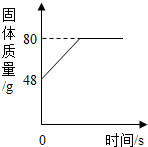

| A、生成物MgO的质量 |
| B、参加反应O2的质量 |
| C、参加反应Mg的质量 |
| D、生成物MgO与参加反应O2的质量和 |