题目内容
 核电荷数为1-18的元素结构示意图等信息如下,回答问题:
核电荷数为1-18的元素结构示意图等信息如下,回答问题: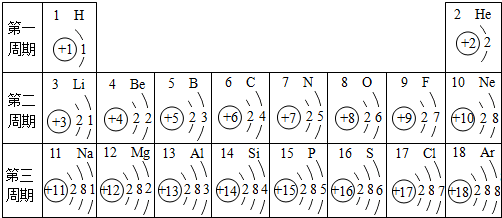
(1)16号元素的原子结构示意图中“8”的含义是
(2)写出地壳中含量最多的元素的符号
(3)写出核外电子排布与10号氖原子相同的阳、阴离子符号各一个:
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,化学式的书写及意义
专题:化学用语和质量守恒定律
分析:(1)根据原子结构示意中各部分的含义来分析解答;以及元素周期表中的一格提供的信息分析;△
(2)根据地壳中元素含量、化学式的书写和推断来分析;
(3)根据阳离子的质子数>核外电子数,阴离子中质子数<电子数;
(2)根据地壳中元素含量、化学式的书写和推断来分析;
(3)根据阳离子的质子数>核外电子数,阴离子中质子数<电子数;
解答:解:(1)由图示可知,16号元素的原子结构示意图中“8”表示硫原子核外第二层电子层数;8号元素与16号元素的最外层电子数相同故化学性质相似;从硫元素的元素周期表中的一格,可以获取原子序数、元素符号、元素名称、相对原子质量;
(2)地壳中含量最多的元素是氧元素;11号元素为钠元素,氧元素与钠元素组成的化合物为氧化钠;
7、8号元素是氮元素和氧元素;设该化合物的化学式为NxOy,则氮元素与氧元素的质量比为
=
,所以
=
,则该化合物为N2O;
(3)核外电子排布与10号氖原子相同的阳离子有钠离子;阴离子有氟离子;氯化钠是由离子构成的化合物;
答案:(1)硫原子核外第二层电子层数;最外层电子数相同;硫元素的相对原子质量是32.06;
(2)O;Na2O;N2O;一氧化二氮;
(3)Na+,F-,NaCl.
(2)地壳中含量最多的元素是氧元素;11号元素为钠元素,氧元素与钠元素组成的化合物为氧化钠;
7、8号元素是氮元素和氧元素;设该化合物的化学式为NxOy,则氮元素与氧元素的质量比为
| 14x |
| 16y |
| 7 |
| 4 |
| x |
| y |
| 2 |
| 1 |
(3)核外电子排布与10号氖原子相同的阳离子有钠离子;阴离子有氟离子;氯化钠是由离子构成的化合物;
答案:(1)硫原子核外第二层电子层数;最外层电子数相同;硫元素的相对原子质量是32.06;
(2)O;Na2O;N2O;一氧化二氮;
(3)Na+,F-,NaCl.
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解原子结构示意图的意义进行分析解题的能力.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
在下列变化中,属于 氧化反应,但不属于化合反应的是( )
| A、硫在氧气中燃烧 |
| B、石蜡在空气中燃烧 |
| C、加热氯酸钾制氧气 |
| D、铁丝在氧气中燃烧 |
下列说法正确的是( )
| A、保持温度不变,向饱和溶液中添加溶质后其溶质质量分数增大 |
| B、饱和溶液降温析出晶体后的溶液仍为饱和溶液 |
| C、从50g 10%的硫酸钠溶液中取出5g,这5g溶液中硫酸钠的质量分数为1% |
| D、在一定温度下,物质X和Y具有相同溶解度,则在该温度下X、Y的饱和溶液中含X、Y两种物质的质量相等 |
某气体既能用排水法收集,又能用向上排空气法收集,则该气体具有的物理性质是( )
| A、难溶于水,密度比空气密度大 |
| B、难溶于水,密度比空气密度小 |
| C、易溶于水,密度比空气密度大 |
| D、易溶于水,密度比空气密度小 |

