题目内容
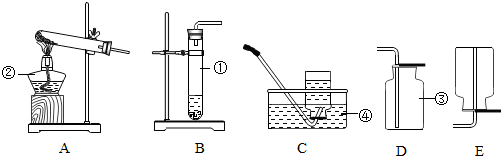
4.甲、乙两同学在学完酸的化学性质后,做了如图所示的实验:
【观察与讨论1】甲同学在做实验时观察到的明显现象是悬浊液变澄清.再滴加无色酚酞溶液,无明显现象(已知CaCl2溶液呈中性).
【观察与讨论2】乙同学在做实验时开始没有观察到气泡产生,于是对碳酸钠能否与盐酸反应表示怀疑.甲同学通过查阅资料得知:在碳酸钠溶液中滴加少量稀盐酸,先发生反应Na2CO3+HCl═NaCl+NaHCO3,继续滴加稀盐酸,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑.所以甲同学认为,乙同学实验时还应,才能观察到有气泡产生.
【观察与讨论3】甲同学先将废液缓慢倒入一洁净的废液杯中,乙同学在观察到气泡产生后,也将实验废液缓慢倒入该废液杯中,没有观察到明显现象.经过讨论确定,甲同学的试管中废液含有的溶质一定有CaCl2,乙同学的试管中废液含有的溶质一定有NaCl(均写化学式).
为了处理实验后产生的废液,甲、乙同学决定对废液杯中最终废液溶质的成分进行探究.
【提出问题】最终废液中含有什么溶质?
【猜想与假设】猜想1:废液中含有CaCl2、NaCl(写化学式)两种溶质.
猜想2:废液中含有CaCl2、NaCl、HCl(写化学式)三种溶质.
猜想3:废液中含有NaHCO3、CaCl2、NaCl三种溶质.
【活动与探究】甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生.
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色.
【结论与反思】(1)猜想2(填“1”或“2”或“3”)正确.
(2)要得到相同的结论,还可采用很多种方法.如加入氧化铁粉末,可观察到溶液呈色,该反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
【表达与交流】甲、乙同学确认了最终废液中溶质的成分,若直接排放,可能造成的危害是腐蚀下水道,你认为处理该废液的方法是将废液中和至中性再排放.
分析 【观察与讨论1】氢氧化钙和稀盐酸反应能生成氯化钙和水;
【观察与讨论2】只有当稀盐酸足量时,碳酸钠溶液才能够和稀盐酸反应生成二氧化碳;
【观察与讨论3】无论氢氧化钙和稀盐酸是否恰好完全反应,形成的溶液中一定含有氯化钙;
无论碳酸钠和稀盐酸的质量如何,形成的溶液中一定含有氯化钠;
【猜想与假设】如果物质之间恰好完全反应时,废液中含有氯化钙和氯化钠;
如果稀盐酸过量时,废液中含有氯化钙、氯化钠和氯化氢;
如果稀盐酸不足,废液中含有碳酸氢钠、氯化钙和氯化钠;
【结论与反思】根据实验现象可以判断废液中溶质的组合情况;
氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的;
【表达与交流】酸性溶液能够腐蚀下水道等.
解答 解:【观察与讨论1】甲同学在做实验时观察到的明显现象是悬浊液变澄清.故答案为:悬浊液变澄清.
【观察与讨论2】乙同学实验时还应继续加入稀盐酸,才能观察到有气泡产生.故答案为:继续加入稀盐酸.
【观察与讨论3】甲同学的试管中废液含有的溶质一定有氯化钙,化学式是CaCl2;
乙同学的试管中废液含有的溶质一定有氯化钠,化学式是NaCl.
故答案为:CaCl2;NaCl.
【猜想与假设】
猜想1:废液中含有CaCl2、NaCl两种溶质;
猜想2:废液中含有CaCl2、NaCl、HCl三种溶质;
故填:CaCl2、NaCl;CaCl2、NaCl、HCl.
【活动与探究】
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生,说明溶液中不含有碳酸氢钠;
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色,说明溶液中含有氯化氢.
【结论与反思】(1)由以上分析可知,猜想2正确.故填:2.
(2)要得到相同的结论,还可采用很多种方法.如加入氧化铁粉末,可观察到溶液呈黄色,该反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
故填:黄; Fe2O3+6HCl═2FeCl3+3H2O.
【表达与交流】若直接排放废液,可能造成的危害是腐蚀下水道等;处理该废液的方法是:将废液中和至中性再排放.
故答案为:腐蚀下水道;将废液中和至中性再排放.
答案:
【观察与讨论1】悬浊液变澄清;
【观察与讨论2】继续加入稀盐酸;
【观察与讨论3】CaCl2;NaCl.
【猜想与假设】CaCl2、NaCl;CaCl2、NaCl、HCl.
【结论与反思】
(1)2;
(2)黄; Fe2O3+6HCl═2FeCl3+3H2O.
【表达与交流】腐蚀下水道;将废液中和至中性再排放.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

| A. | 水沸腾:试管底部产生气泡,试管口有白烟产生 | |
| B. | 胆矾研碎:蓝色块状固体变成蓝色粉末状固体 | |
| C. | 向硫酸铜溶液中滴加氢氧化钠溶液后并加热:溶液中产生蓝色沉淀,加热后产生黑色固体 | |
| D. | 石灰石和稀盐酸反应:白色固体表面产生了大量的二氧化碳 |
| A. | 原子的质量主要集中在原子核上 | |
| B. | 在化学变化中原子不变 | |
| C. | 保持氧气化学性质的最小微粒是氧分子 | |
| D. | 分子大,原子小 |
| A. | 食醋 | B. | 牛奶 | C. | 食盐水 | D. | 牙膏或肥皂水 |
| A. |  配制稀硫酸 | B. |  制备氢气 | ||
| C. |  收集氢气 | D. |  氢气还原氧化铜 |
| A. | 把溶液的量倒掉一半 | |
| B. | 溶质的质量增大一倍 | |
| C. | 将100g10%的盐酸与200g25%的盐酸混合 | |
| D. | 蒸发掉50g溶剂 |