题目内容
5.Na2SO4是制作纸张、药品、染料稀释剂等的重要原料.某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图1所示.
(1)加入NaOH溶液可除去的阳离子是Mg2+(填离子符号),其反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl.
若添加的NaOH和Na2CO3添加过量,可加入适量稀硫酸(填名称)除去.
(2)溶液M中的溶质是Na2SO4和杂质NaCl,观察图2的溶解度曲线,则操作b是:先将溶液M蒸发浓缩,在降温结晶、过滤,降温结晶的最佳温度范围是30℃以下,因为Na2SO4的溶解度在30℃以下比氯化钠小.
分析 (1)据本题给出的除去杂质选用的试剂,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,写出反应的化学方程式即可;如果氢氧化钠和碳酸钠过量,可加入适量的稀硫酸,稀硫酸和氢氧化钠反应生成硫酸钠和水,稀硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂的原则.
(2)根据硫酸钠和氯化钠的溶解度曲线变化分析.
解答 解:(1)由于加入的氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,因此除去的是MgCl2,反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;稀硫酸和氢氧化钠反应生成硫酸钠和水,没有带入新杂质;碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳气体,没有带入任何其它杂质;符合除杂的原则,故NaOH和Na2CO3如果添加过量了,可在过滤后向滤液中滴加稀硫酸除去.
(2)由于硫酸钠的溶解度在30℃以下比氯化钠小,降温的过程中会析出大量的硫酸钠;
故答为:(1)Mg2+,2NaOH+MgCl2═Mg(OH)2↓+2NaCl,稀硫酸;(2)30,在30℃以下比氯化钠小.
点评 本题综合性较强,掌握盐的化学性质、化学方程式的书写、过滤操作及抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)等是正确解答本题的关键.

练习册系列答案
相关题目
6.下列物品所含的主要材料,不属于合成材料的是( )
| A. | 涤纶衣 | B. | 塑料杯 | C. | 铁桶 | D. | 尼龙袜 |
13.下列有关主题知识的归纳完全正确的是( )
| A.安全常识 室内煤气泄漏-立即打开排风扇 浓硫酸沾到皮肤上-立即用水清洗 | B.化学与环境 减少白色污染-使用可降解塑料 减少酸雨-开发绿色新能源 |
| C.生活常识 洗涤剂洗去油污-乳化作用 把硬水转化成软水-过滤 | D.关于“舌尖上的化学” 真空包装-防止氧化而变质 延长食品保质期-添加大量防腐剂 |
| A. | A | B. | B | C. | C | D. | D |
20.H2S、S、M、SO3四种物质是按硫元素化合价由低到高顺序排列的.其中M这种物质的化学式可能是( )
| A. | Na2SO4 | B. | H2SO4 | C. | Na2S | D. | H2SO3 |
10.下列说法正确的是( )
| A. | 生石灰制成的食品干燥剂可以食用 | |
| B. | 直接品尝实验室药品的味道 | |
| C. | 利用硝酸铵溶于水吸热的原理,自制冰袋给发烧病人降温 | |
| D. | 液化气起火,迅速关闭阀门,以断绝可燃物的来源 |
17.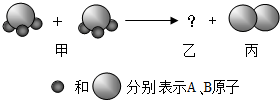 如图所示,两个甲分子反应生成X个乙分子和Y个内分子,则从图示获得的信息中,正确的是( )
如图所示,两个甲分子反应生成X个乙分子和Y个内分子,则从图示获得的信息中,正确的是( )
 如图所示,两个甲分子反应生成X个乙分子和Y个内分子,则从图示获得的信息中,正确的是( )
如图所示,两个甲分子反应生成X个乙分子和Y个内分子,则从图示获得的信息中,正确的是( )| A. | 分子的种类在化学反应中未发生了改变 | |
| B. | 该反应的反应类型为置换反应 | |
| C. | 反应生成的物质丙属于单质 | |
| D. | X与Y之比等于1:3 |
15.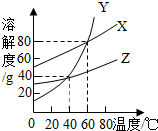 X、Y、Z三种物质的溶解度曲线如图所示.下列叙述中,正确的是( )
X、Y、Z三种物质的溶解度曲线如图所示.下列叙述中,正确的是( )
 X、Y、Z三种物质的溶解度曲线如图所示.下列叙述中,正确的是( )
X、Y、Z三种物质的溶解度曲线如图所示.下列叙述中,正确的是( )| A. | 40℃时Z的溶解度最大 | |
| B. | 温度由60℃降至40℃时,Y析出的晶体最多 | |
| C. | 40℃时,Z和Y的饱和溶液的溶质质量分数相同 | |
| D. | 40℃时,X、Y、Z的饱和溶液升温至60℃,溶质质量分数X=Y>Z |