题目内容
18.目前部分农村的饮用水主要还是地下水,饮用遭到污染或硬度大的地下水不利于人体健康,政府积极建设自来水厂,让农民喝上清洁的水.(1)测定地下水的酸碱度可用pH试纸;
(2)自来水生产过程中,可用过滤的方法除去水中不溶性杂质,同时还必须进行消毒.X是一种新型的自来水消毒剂,工业上制取X的化学方程式为:Cl2+2NaClO2═2NaCl+2X,则X的化学式为ClO2.
分析 (1)根据使用pH试纸可以测试溶液的酸碱度;进行解答;
(2)过滤是除去水中不溶性杂质的一种方法;根据在化学反应中原子的种类、原子的数目不变判断物质的化学式.
解答 解:
(1)测定溶液的酸碱度应使用pH试纸,所以测定地下水的酸碱度可用:pH试纸;
(2)过滤是除去水中不溶性杂质的一种方法;
根据质量守恒定律,在化学方程式为:Cl2+2NaClO2═2NaCl+2X中反应前氯原子有4个,钠原子有2个,氧原子有4个,而反应后氯化钠中钠原子有2个,氯原子有2个,所以2M中应有2个氯原子,4个氧原子,所以X的化学式为ClO2;
故答案为:
(1)pH试纸
(2)过滤;ClO2.
点评 本考点考查了过滤的方法、质量守恒定律等,属于结合课本知识的信息.一定要加强记忆,综合应用.本考点主要出现在填空题和选择题中.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
11.下列变化中,属于化学变化的是( )
| A. | 胆矾研碎 | B. | 木炭燃烧 | C. | 石蜡熔化 | D. | 衣服晾干 |
12.某个化学反应的微观示意图如图.有关说法正确的是( )
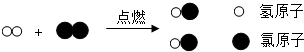

| A. | 该反应为分解反应 | |
| B. | 该反应不遵守质量守恒定律 | |
| C. | 该反应前后分子种类未发生变化 | |
| D. | 该反应的化学方程式为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl |
10.下列各组物质中均含有少量杂质(括号内的物质为杂质),现在要求将各物质中的杂质除去,如表中选用的试剂及操作方法都正确的是( )
| 组别 | 被提纯的物质 | 所选试剂及操作方法 |
| A | KCl固体(MnO2固体) | 溶解、过滤、洗涤、干燥 |
| B | CO2(HCl气体) | 通过盛NaOH溶液的洗气瓶 |
| C | CaO固体(CaCO3固体) | 加入稀盐酸再蒸发 |
| D | NaOH溶液[Ca(OH)2溶液] | 加入适量的Na2CO3溶液再过滤 |
| A. | A | B. | B | C. | C | D. | D |
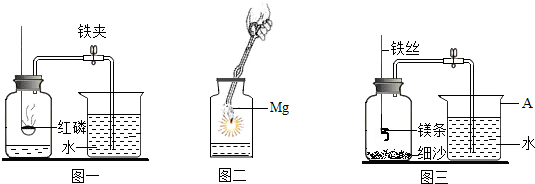
 已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示.
已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示.