题目内容
11.下列用字母表示的物质由H、C、O、Na、Cl、Ca、Fe中的一种或几种元素组成,它们是初中化学常见的物质.(1)A在生命活动中可供给呼吸,则A的化学式为O2.
(2)B是一种常见的金属单质,与C溶液混合后生成一种在标准状况下密度最小的气体,则B与C反应的化学方程式为Fe+2HCl=FeCl2+H2↑.
(3)D具有强烈的腐蚀性,易潮解.与C溶液混合时需借助指示剂来证明反应发生,则D与C 反应的化学方程式为NaOH+HCl=NaCl+H2O.
(4)E用于玻璃、造纸、纺织、洗涤剂的生产,其溶液可与C溶液反应,也可与F溶液混合生成D,E生成D的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.将上述两个反应后的所有物质倒在同一个废液缸中,废液澄清透明,此时废液中的溶质组成为NaCl、CaCl2和HCl;NaCl、CaCl2.(写出所有可能)
分析 (1)A在生命活动中可供给呼吸,因此A是氧气;
(2)B是一种常见的金属单质,与C溶液混合后生成一种在标准状况下密度最小的气体-氢气,因此是金属和酸的反应;
(3)D具有强烈的腐蚀性,易潮解,因此D是氢氧化钠,与C溶液混合时需借助指示剂来证明反应发生,说明氢氧化钠和酸反应无现象,据此分析;
(4)E用于玻璃、造纸、纺织、洗涤剂的生产,其溶液可与C-盐酸溶液反应,也可与F溶液混合生成D-氢氧化钠,因此E是碳酸钠,碳酸钠和氢氧化钙反应产生碳酸钙沉淀和氢氧化钠,因此F是氢氧化钙;根据实验的现象结合反应的程度分析废液中的溶质成分.
解答 解:(1)A在生命活动中可供给呼吸,因此A是氧气,故答案为:O2;
(2)B是一种常见的金属单质,与C溶液混合后生成一种在标准状况下密度最小的气体,因此可以是铁和盐酸的反应产生氯化亚铁和氢气,故反应的方程式为:Fe+2HCl=FeCl2+H2↑;
(3)D具有强烈的腐蚀性,易潮解,因此D是氢氧化钠,与C溶液混合时需借助指示剂来证明反应发生,说明氢氧化钠和酸反应无现象,因此C是盐酸,故反应的方程式为:NaOH+HCl=NaCl+H2O;
(4)E用于玻璃、造纸、纺织、洗涤剂的生产,其溶液可与C-盐酸溶液反应,也可与F溶液混合生成D-氢氧化钠,因此E是碳酸钠,碳酸钠和氢氧化钙反应产生碳酸钙沉淀和氢氧化钠,因此F是氢氧化钙,故反应的方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;碳酸钠和盐酸反应一定会生成氯化钠,将上述两个反应后的所有物质倒在同一个废液缸中,废液澄清透明,说明碳酸钙溶于过量的盐酸会产生氯化钙,反应后盐酸可能过量,也可能恰好反应,因此溶液中的溶质可能是NaCl、CaCl2和HCl;NaCl、Ca Cl2;故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;NaCl、CaCl2和HCl;NaCl、CaCl2.
点评 本题考查了常见物质的用途以及物质之间的相互反应,完成此题,可以依据已有的知识结合题干提供的信息进行推断分析,要求同学们在平时的学习中加强基础知识的储备,以便灵活应用.

 阅读快车系列答案
阅读快车系列答案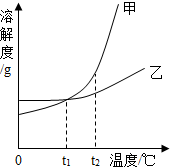
| A. | t1℃时,甲和乙溶液中溶质的质量分数一定相等 | |
| B. | t2℃时,分别用等质量的甲和乙固体,完全溶解配制成饱和溶液,得到乙溶液的质量大于甲 | |
| C. | 将甲、乙的饱和溶液从t1℃升温至t2℃,甲溶液中溶质的质量分数比乙大 | |
| D. | 使甲的不饱和溶液变成饱和溶液只能用降温的方法 |
| A. | 青蒿素是一种有机物 | B. | 青蒿素中氢、氧的质量比为11:40 | ||
| C. | 青蒿素中含有42个原子 | D. | 青蒿素中碳元素质量分数最大 |
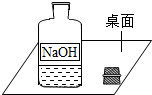 同学们来到化学实验室,意外看到了一个不和谐的“音符”(如图).由此,激发了同学们的探究欲望.
同学们来到化学实验室,意外看到了一个不和谐的“音符”(如图).由此,激发了同学们的探究欲望.(1)同学们取该瓶中少量溶液滴加稀盐酸,看到冒气泡,说明药品已变质,变质反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
【进行猜想】小天的猜想:NaOH 溶液部分变质;
你的猜想:NaOH溶液全部变质.
【实验探究】小天设计如下实验来验证自己的猜想,请完成下表:
| 探究步骤 | 预计现象 | 探究目的 |
| ①:取少量溶液于试管中,滴加足量的CaCl2试剂 | 出现白色沉淀 | 除尽溶液中的CO32- |
| ②:向实验①过滤后所得溶液中滴加酚酞试液 | 试液变红 | 证明溶液中尚存NaOH |
(2)小天第二次滴加的试剂除用指示剂外,还可以用CuSO4溶液替代.
| A. | 用甲醛水溶液浸泡水产品以延长保鲜期 | |
| B. | 将工业用盐(如NaNO2)用于烹调 | |
| C. | 服用氢氧化钠治疗胃酸过多 | |
| D. | 用肥皂水区分硬水和软水 |
| A. | O2 | B. | N2 | C. | SO2 | D. | CO2 |
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 | |
| 小东 | 用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH | pH试纸变色 pH>7(填“>”或“<”) | 该溶液是氢氧化钠溶液 |
| 小南 | 取适量溶液于试管中,加入经打磨过的铝条 | 有气泡产生 | 该溶液是稀硫酸 |
【解决问题】小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是产生蓝色沉淀,于是一致认为该溶液是氢氧化钠溶液,为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量.实验设计如下:
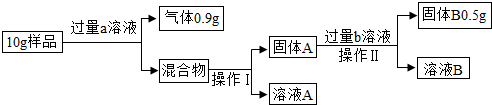
【回答问题】
(1)写出操作Ⅰ中玻璃棒的作用:引流.
(2)a溶液是氢氧化钠溶液.
(3)金属铜的质量为0.5g,固体A含有的物质是镁和铜,溶液A中所含溶质是NaOH、NaAlO2.
| A. | 气凝胶常温下氧化学性质很不稳定 | |
| B. | 气凝胶具有很强的吸附作用 | |
| C. | 气凝胶是一种化合物 | |
| D. | 气凝胶在氧气中完全燃烧的产物是CO2 |