题目内容
6.请根据下列装置图,回答有关问题.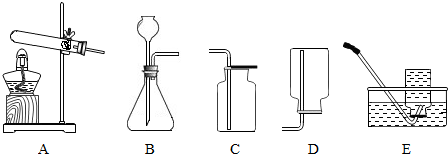
(1)写出实验室用过氧化氢制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选择的发生装置为B(填字母).
(2)写出实验室用锌和稀硫酸制取氢气的化学方程式Zn+H2SO4=ZnSO4+H2↑,要获得较纯净的氢气选择的收集装置为E(填字母).
(3)用质量分数为36.5%的浓盐酸配制一定质量的溶质质量分数为20%的稀盐酸,配制的主要步骤是计算、量取、溶解稀释.该溶液配制过程中除用到量筒、玻璃棒和烧杯外,还需要的仪器是胶头滴管.
(4)实验室要制取8.8g二氧化碳,至少需要多少克质量分数为20%的稀盐酸与足量大理石反应?(在答卷纸上写出计算过程)73g.
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(3)溶液稀释前后,溶质质量不变;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,根据二氧化碳的质量可以计算氯化氢的质量,进一步可以计算稀盐酸的质量.
解答 解:(1)实验室用过氧化氢制取氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,反应不需要加热,应该用B装置作为发生装置;
(2)实验室用锌和稀硫酸制取氢气的化学方程式为:Zn+H2SO4=ZnSO4+H2↑,要获得较纯净的氢气,应该用排水法收集,即选择的收集装置为E;
(3)配制的主要步骤是计算、量取、溶解稀释;
该溶液配制过程中除用到量筒、玻璃棒和烧杯外,还需要的仪器是胶头滴管;
(4)设至少需要质量分数为20%的盐酸的质量为x,
CaCO3+2HCl═CaCl2+CO2↑+H2O,
73 44
x×20% 8.8g
$\frac{73}{x×20%}$=$\frac{44}{8.8g}$,
x=73g,
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;Zn+H2SO4=ZnSO4+H2↑;E;溶解稀释;胶头滴管;73g.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
14.下列有关溶液的说法正确的是( )
| A. | 对某不饱和溶液进行蒸发溶剂后一定会得到其饱和溶液 | |
| B. | 溶液都是均一、稳定且无色的混合物 | |
| C. | 不饱和溶液转化为饱和溶液,溶质质量分数可能不变 | |
| D. | 浓溶液可能为不饱和溶液,不饱和溶液一定是稀溶液 |
1.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | HCl( CO2) | 适量NaOH溶液 | 洗气 |
| B | 氢气(水蒸气) | 浓硫酸 | 洗气 |
| C | CO2(CO) | 足量O2 | 点燃 |
| D | 稀盐酸(稀硫酸) | 适量硝酸钡溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
18.2014年4月兰州发生了自来水苯超标事故,引起人们对水安全的关注.己知苯的化学式为C6H6,下列有关说法正确的是 ( )
| A. | 笨分子中碳的原子结构示意图为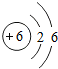 | |
| B. | 苯分子是由6个碳元素和6个氢元素组成 | |
| C. | 苯中的C、H元素的质量比为12:1 | |
| D. | 苯中碳、氢元素均位于元素周期表的第二周期 |
15.下列俗称与化学式对应不正确的是( )
| A. | 小苏打:NaHCO3 | B. | 苏打:Na2CO3 | C. | 纯碱:NaOH | D. | 熟石灰:Ca(OH)2 |
16.以下是初中化学中的一些基本经验,不能达到实验目的是( )
| A. | 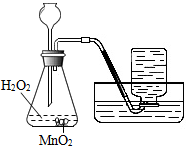 制取氧气 | B. | 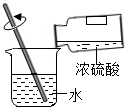 稀释浓硫酸 | ||
| C. | 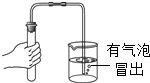 检查装置气密性 | D. | 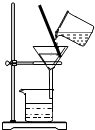 粗盐过滤 |
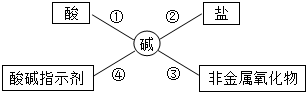 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题:
酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的腐蚀性,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题: