题目内容
某同学用无水氯化钙来测定某未知质量分数的Na2CO3溶液.该实验发生反应的化学方程式为:Na2CO3+CaCl2═2NaCl+CaCO3↓.其中五次实验结果如表所示:
(1)反应中碳酸钠有剩余的有 (选填序号).
(2)表中x的值是 .
(3)试计算碳酸钠溶液中溶质的质量分数.
| 实验次数 | 氯化钙质量/g | 碳酸钠溶液的质量/g | 碳酸钙的质量/g |
| 1 | 5.55 | 200 | 5 |
| 2 | 11.1 | 200 | 10 |
| 3 | 22.2 | 200 | 20 |
| 4 | 33.3 | 250 | 25 |
| 5 | 55.5 | 400 | x |
(2)表中x的值是
(3)试计算碳酸钠溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:分析比较表中的数据:前3次Na2CO3溶液到位质量都是200克,随着氯化钙质量的倍数增加,生成的碳酸钙的质量也在成倍数增加,可以得出前3次氯化钙全部参加了反应,氯化钙质量与碳酸钙的质量比为5.55:5.当在第4次氯化钙的质量增加到是第一次6倍时,这时生成的碳酸钙的质量只是第一次的5倍,说明了250克碳酸钠溶液中溶质全部参加了反应,生成了碳酸钙是25克,可得出碳酸钠溶液与碳酸钙的质量比为250:25=50:5,由此可以得出氯化钙质量、碳酸钠溶液质量、碳酸钙质量比为:5.55:50:5,有这个质量比带入到上述表中分析有关数据,很容易看出:前两次碳酸钠溶液有剩余,第3次氯化钙和碳酸钠溶液是恰好反应,X的值是40克.由第3次的有关数据,可以计算出碳酸钠溶液中溶质的质量分数.
解答:解:
通过分析、比较表中的数据可看出:随着氯化钙质量的倍数增加,生成的碳酸钙的质量也在成倍数增加,可以得出前3次氯化钙全部参加了反应,氯化钙质量与碳酸钙的质量比为5.55:5.当在第4次氯化钙的质量增加到第一次6倍时,这时生成的碳酸钙的质量只是第一次的5倍,说明了250克碳酸钠溶液中的溶质全部参加了反应,生成了碳酸钙是25克,可得出碳酸钠溶液与碳酸钙的质量比为250:25=50:5,由此可以得出氯化钙、碳酸钠溶液、碳酸钙的质量比为:5.55:50:5,有这个质量比带入到上述表中分析有关数据,很容易看出:
(1)前两次碳酸钠溶液有剩余
(2)第3次氯化钙和碳酸钠溶液是恰好反应,X的值是40克.
通过上述分析,已经知道在第3次试验中,22.2克的氯化钙与200克的碳酸钠溶液是恰好反应,生成了20克地碳酸钙沉淀,利用这些数据就可以计算出碳酸钠溶液中溶质的质量分数.
(3)设200 g的Na2CO3溶液中Na2CO3的质量为m.
Na2CO3+CaCl2═2NaCl+CaCO3↓
106 100
m 20 g
=
解得m=
=21.2 g
碳酸钠溶液中溶质的质量分数为:
×100%%=10.6%
答案:
(1)1、2
(2)40
(3)碳酸钠溶液中溶质的质量分数是10.6%.
通过分析、比较表中的数据可看出:随着氯化钙质量的倍数增加,生成的碳酸钙的质量也在成倍数增加,可以得出前3次氯化钙全部参加了反应,氯化钙质量与碳酸钙的质量比为5.55:5.当在第4次氯化钙的质量增加到第一次6倍时,这时生成的碳酸钙的质量只是第一次的5倍,说明了250克碳酸钠溶液中的溶质全部参加了反应,生成了碳酸钙是25克,可得出碳酸钠溶液与碳酸钙的质量比为250:25=50:5,由此可以得出氯化钙、碳酸钠溶液、碳酸钙的质量比为:5.55:50:5,有这个质量比带入到上述表中分析有关数据,很容易看出:
(1)前两次碳酸钠溶液有剩余
(2)第3次氯化钙和碳酸钠溶液是恰好反应,X的值是40克.
通过上述分析,已经知道在第3次试验中,22.2克的氯化钙与200克的碳酸钠溶液是恰好反应,生成了20克地碳酸钙沉淀,利用这些数据就可以计算出碳酸钠溶液中溶质的质量分数.
(3)设200 g的Na2CO3溶液中Na2CO3的质量为m.
Na2CO3+CaCl2═2NaCl+CaCO3↓
106 100
m 20 g
| 106 |
| 100 |
| m |
| 20g |
解得m=
| 106×20g |
| 100 |
碳酸钠溶液中溶质的质量分数为:
| 21.2g |
| 200g |
答案:
(1)1、2
(2)40
(3)碳酸钠溶液中溶质的质量分数是10.6%.
点评:本题属于数据处理型计算习题,这种题型是近年来在各地中考试题中出现的一种新题型.这类题符合当今信息社会发展的趋势,要求同学们具有在多项信息中提取所需,进行分析和解决问题的能力.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目


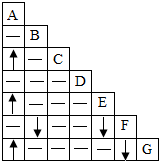 A~G分别为Fe、CO2、稀盐酸、澄清的石灰水、NaOH溶液、Na2CO3溶液、NaHCO3溶液中的一种,根据它们之间混合时的现象(如图所示,图中“↑”代表有气体生成,“↓”代表有沉淀生成,“-”代表反应中无明显现象或不反应)回答问题.
A~G分别为Fe、CO2、稀盐酸、澄清的石灰水、NaOH溶液、Na2CO3溶液、NaHCO3溶液中的一种,根据它们之间混合时的现象(如图所示,图中“↑”代表有气体生成,“↓”代表有沉淀生成,“-”代表反应中无明显现象或不反应)回答问题.