题目内容
11.下列说法正确的是( )| A. | PH=0的溶液显中性,不能使酚酞变色 | |
| B. | 正常雨水的PH为7,酸雨的PH<7 | |
| C. | CO2气体中有水蒸气,可以用氢氧化钠溶液干燥 | |
| D. | 工业废气中的二氧化硫,可以用石水浆吸收处理,防止空气污染 |
分析 A、pH=7的溶液是中性溶液;
B、正常雨水的PH为5.6,当雨水的酸碱度达到一定程度时,便形成酸雨;
C、根据氢氧化钠的性质分析;
D、根据碱的性质分析.
解答 解:A、pH=0的溶液是酸性溶液,故错误;
B、pH<5.6的雨水属于酸雨.不正确.
C、二氧化碳属于酸性气体,氢氧化钠能与其反应,也不能用来干燥该气体,故错误;
D、二氧化硫能与氢氧化钙反应,工业废气中的二氧化硫,可以用石水浆吸收处理,防止空气污染,正确;
故选:D.
点评 本题溶液的酸碱性与pH值碱的关系,酸雨的pH值及碱的应用,难度不大.

练习册系列答案
相关题目
2.下列有关生活中化学知识的说法,正确的是( )
| A. | 纯棉床单、塑料包装袋、电木插座等都属于有机合成材料 | |
| B. | 糖类和油脂在人体内转化后能为机体供能 | |
| C. | 钙、铁、铅都是人体必需的微量元素 | |
| D. | 生活中常用甲醛浸泡水产品,达到保鲜的目的 |
19.下列的陈述中Ⅰ、Ⅱ的因果关系正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 生石灰易与水反应 | 生石灰常用作食品干燥剂 |
| B | 氢气是最轻的气体 | 点燃氢气前要验纯 |
| C | 二氧化碳用于灭火 | 二氧化碳没有毒性 |
| D | 取液时试剂瓶塞倒放在桌面上 | 液体药品盛放在细口瓶 |
| A. | A | B. | B | C. | C | D. | D |
6.下列说法正确的是( )
| A. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| B. | 侯德榜制碱法,制出的火碱又叫烧碱 | |
| C. | 花香四溢,说明分子在不断地运动 | |
| D. | 铝比铁的抗锈蚀性能强,说明铝的金属活动性比铁弱 |
3.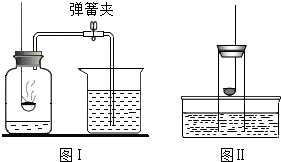 下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
 下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是( )| A. | 不能用木炭代替红磷 | |
| B. | 图II所示装置也可以测定空气中氧气含量 | |
| C. | 图I中进入集气瓶的水约占烧杯中水的五分之一 | |
| D. | 氮气不与红磷反应且难溶于水,是设计该实验的依据之一 |
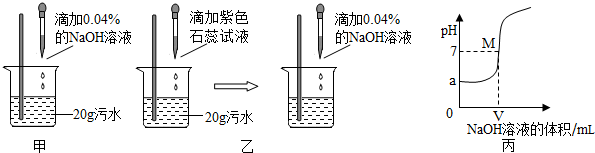
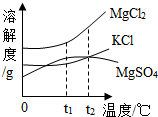 食盐在生产和生活中具有广泛的用途.
食盐在生产和生活中具有广泛的用途.