题目内容
12.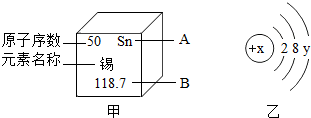 如图的甲是某元素在元素周期表中的部分信息,乙是某微粒的结构示意图.请根据图中信息回答问题:
如图的甲是某元素在元素周期表中的部分信息,乙是某微粒的结构示意图.请根据图中信息回答问题:(1)图甲中A表示元素符号,B表示相对原子质量.
(2)若图乙中当x-y=10时,该微粒是原子(填“阴离子”、“阳离子”或“原子”),若y=8时,该微粒带有两个单位的负电荷,则x=16.
分析 (1)根据元素周期表的信息来分析;(2)根据微粒的判断方法以及不同微粒中质子数与电子数的关系来分析.
解答 解:(1)在元素周期表中,右上角的符号表示该元素的元素符号,下方的数字表示该元素的相对原子质量;故填:元素符号;相对原子质量;
(2)因为x-y=10,即x=10+y,微粒核内的质子数=核外电子数,故乙是原子;当y=8时,该微粒带有两个单位的负电荷,也就是得到了2个电子,故x=2+8+8-2=16.
故答案为:原子;16.
点评 本题考查学生对周期表中的信息和粒子结构示意图的有关知识,重点是对相关知识的掌握及应用的能力的训练.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
2.已知:Al(OH)3可与NaOH溶液反应,生成能溶于水的NaAlO2,即:Al(OH)3+NaOH=NaAlO2+2H2O,Mg(OH)2不与NaOH溶液反应,Mg(OH)2═MgO+H2O.现将ag镁铝合金粉末溶于足量的盐酸中,再加过量的氢氧化钠溶液,过滤,将沉淀进行洗涤、干燥、充分灼烧,得到白色粉末的质量还是ag,则原合金中镁的质量分数为( )
| A. | 60% | B. | 70% | C. | 80% | D. | 无法确定 |
3.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 向澄清石灰水中通入少量的CO2:Ca(OH)2+CO2=CaCO3↓+H2O 复分解反应 | |
| B. | 用稀硫酸洗去附着在试管壁上的铜:Cu+H2SO4=CuSO4+H2↑ 置换反应 | |
| C. | 铁丝在氧气中燃烧的反应:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 化合反应 | |
| D. | 工业制取二氧化碳:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 |
20.下列关于水的叙述错误的是( )
| A. | 水的电解实验证明水是由氢元素和氧元素组成 | |
| B. | 我国水资源总量居世界第六位 | |
| C. | 生活中通过煮沸可降低水的硬度 | |
| D. | 活性炭能吸附河水里的所有杂质 |
7.某黄铜仅由铜和锌组成,为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
认真分析数据,回答下列问题:
(1)黄铜中铜的质量分数为70%;
(2)所用稀硫酸的溶质质量分数;
(3)恰好完全反应时,溶液中溶质的质量分数.
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)黄铜中铜的质量分数为70%;
(2)所用稀硫酸的溶质质量分数;
(3)恰好完全反应时,溶液中溶质的质量分数.
2.下列实验操作中,正确的是( )
| A. |  熄灭酒精灯 | B. | 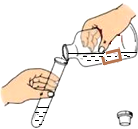 液体取用 | C. | 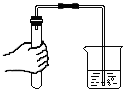 检查气密性 | D. | 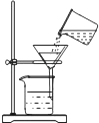 过滤 |